سرطان معده | از علائم تا درمان
- 2026-02-19
- 0 Likes
- 0 Comments
سرطان معده چیست؟
سرطان معده (به انگلیسی: Stomach cancer یا Gastric cancer) نوعی سرطان بدخیم است که از سلولهای پوشش داخلی معده (مخاط معده) شروع میشود. در این بیماری، سلولهای طبیعی معده دچار تغییرات غیرطبیعی (جهش DNA) میشوند، رشد و تقسیم کنترلنشده پیدا میکنند و بهتدریج توده یا تومور سرطانی تشکیل میدهند.
این تومور ابتدا در لایه داخلی معده (مخاط) شکل میگیرد و اگر درمان نشود، به لایههای عمیقتر دیواره معده نفوذ کرده و ممکن است به غدد لنفاوی اطراف، کبد، ریهها، استخوانها یا صفاق (دیواره شکم) گسترش یابد (متاستاز).
آناتومی و عملکرد معده
معده یکی از مهمترین اندامهای دستگاه گوارش است که نقش کلیدی در هضم اولیه غذا دارد. شناخت ساختار و عملکرد آن کمک میکند تا بفهمیم چرا سرطان معده اغلب از لایه داخلی (مخاط) شروع میشود و چگونه به لایههای عمیقتر نفوذ میکند.
جایگاه معده در بدن
معده در قسمت فوقانی شکم (یکچهارم بالایی سمت چپ حفره شکمی) قرار دارد، زیر دیافراگم، بین مری (بالا) و دوازدهه (اولین بخش روده کوچک، پایین). شکل آن شبیه حرف J انگلیسی یا کیسهای قابل انبساط است و در حالت خالی کوچک، اما میتواند تا ۱–۴ لیتر غذا (در بزرگسالان) را نگه دارد.
بخشهای اصلی معده
معده به چهار بخش اصلی تقسیم میشود:
- کاردیا (Cardia): بخش بالایی که به مری متصل است. اسفنکتر تحتانی مری (LES) اینجا قرار دارد و از بازگشت اسید به مری جلوگیری میکند.
- فوندوس (Fundus): بخش گنبدیشکل بالای معده، اغلب حاوی هوا (حباب گاز معده).
- بدن یا تنه (Body/Corpus): بخش اصلی و بزرگترین قسمت، جایی که بیشتر هضم شیمیایی رخ میدهد.
- پیلور (Pylorus): بخش پایینی شامل آنتروم (Antrum) و کانال پیلوریک. اسفنکتر پیلور (Pyloric sphincter) اینجا غذا را بهتدریج به روده کوچک میفرستد.
لایههای دیواره معده (از داخل به خارج)
دیواره معده چهار لایه اصلی دارد که درک آنها برای فهم گسترش سرطان ضروری است:
- مخاط (Mucosa): لایه داخلی، پوشیده از سلولهای اپیتلیال استوانهای و غدد معده. شامل:
- سلولهای اصلی (Chief cells): ترشح پپسینوژن (پیشساز پپسین برای هضم پروتئین).
- سلولهای جداری (Parietal cells): ترشح اسید هیدروکلریک (HCl) و فاکتور داخلی (برای جذب ویتامین B12).
- سلولهای مخاطی: ترشح مخاط محافظ برای جلوگیری از خودهضمی معده.
- سلولهای انتروکرین (مانند سلولهای G): ترشح هورمونهایی مثل گاسترین.
این لایه جایی است که سرطان معده (بهویژه آدنوکارسینوم) معمولاً از آن شروع میشود.
- زیرمخاط (Submucosa): بافت همبند سست با رگهای خونی، لنفاوی و شبکه عصبی مایسنر.
- عضلانی (Muscularis externa): سه لایه عضله صاف (طولی خارجی، حلقوی میانی، مورب داخلی) که حرکات مخلوطکننده و پریستالتیک را ایجاد میکند.
- سروزا (Serosa): لایه خارجی از صفاق احشایی که معده را میپوشاند و به اندامهای مجاور متصل میکند.
عملکردهای اصلی معده
معده سه نقش کلیدی دارد که اختلال در آنها میتواند به مشکلات گوارشی و سرطان منجر شود:
- ذخیرهسازی موقت غذا: غذا را برای چند ساعت نگه میدارد تا بهتدریج هضم شود (ظرفیت ۱–۴ لیتر).
- هضم مکانیکی: با انقباضات عضلانی قوی، غذا را مخلوط و آسیاب میکند تا به کیموس (ماده نیمهمایع) تبدیل شود.
- هضم شیمیایی: ترشح اسید معده (pH ۱–۴)، پپسین (برای پروتئینها)، لیپاز معده (برای چربیها) و مخاط محافظ. همچنین هورمون گاسترین ترشح میشود که اسید را تحریک میکند.
در سرطان معده، تومور اغلب از مخاط شروع شده، به زیرمخاط و عضلانی نفوذ میکند، سپس به سروزا رسیده و میتواند به غدد لنفاوی، کبد یا صفاق متاستاز دهد. عفونت هلیکوباکتر پیلوری باعث التهاب مزمن مخاط (گاستریت) میشود که پیشساز اصلی سرطان است.
انواع سرطان معده
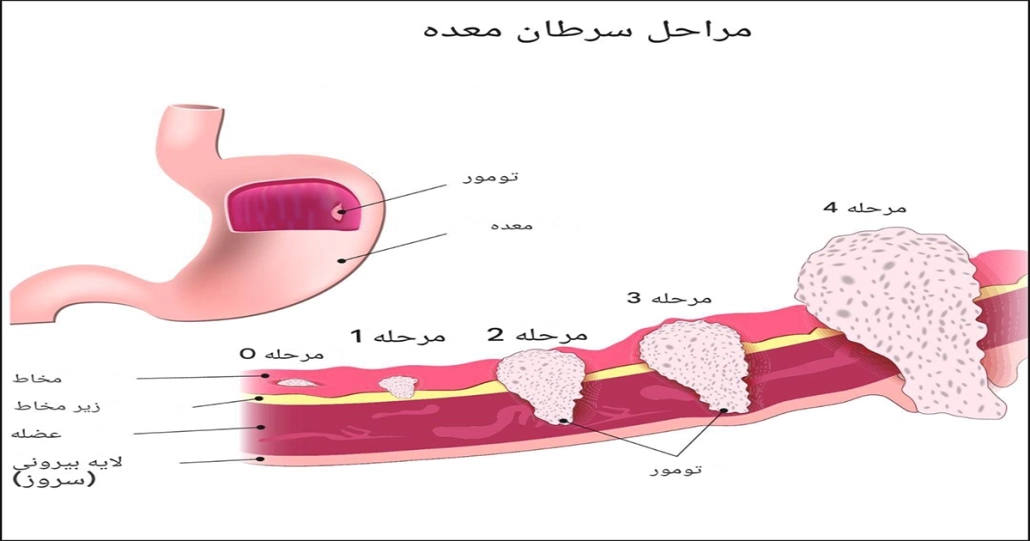
سرطان معده بر اساس نوع سلولهایی که از آنها شروع میشود، به انواع مختلفی تقسیمبندی میگردد. شایعترین نوع آن آدنوکارسینوم است که بیش از ۹۰–۹۵٪ موارد را تشکیل میدهد. انواع نادرتر رفتار، درمان و پیشآگهی متفاوتی دارند.
۱. آدنوکارسینوم معده – شایعترین نوع
این سرطان از سلولهای غدهای لایه مخاطی (داخلیترین لایه) معده شروع میشود و حدود ۹۰–۹۵٪ کل سرطانهای معده را شامل میشود.
طبقهبندی لورن (Lauren classification) – رایجترین تقسیمبندی بالینی:
- نوع رودهای (Intestinal type): شایعتر، معمولاً در قسمتهای پایین معده (آنتروم یا بدن)، مرتبط با التهاب مزمن (مانند عفونت هلیکوباکتر پیلوری، رژیم پرنمک، سیگار). سلولها شبیه سلولهای روده هستند، رشد آهستهتر، اغلب در مردان مسنتر دیده میشود و پیشآگهی نسبتاً بهتر دارد.
- نوع منتشر یا پراکنده (Diffuse type): تهاجمیتر، سریعتر رشد میکند، اغلب در کل معده پخش میشود، کمتر به عوامل محیطی وابسته، گاهی ارثی (مانند سندرمهای ژنتیکی مانند CDH1 mutation). سلولها پراکنده و کمتر چسبنده هستند (شامل زیرنوع signet-ring cell carcinoma با سلولهای حلقهدار).
۲. تومورهای استرومایی دستگاه گوارش
- نوع نادر (حدود ۱–۳٪ سرطانهای معده).
- از سلولهای خاص بینابینی کاژال (Interstitial cells of Cajal) در دیواره عضلانی یا زیرمخاطی معده شروع میشود.
- نوعی سارکوم بافت نرم است (نه آدنوکارسینوم).
- اغلب در معده شایعتر از سایر نقاط GI tract.
- رشد آهسته تا متوسط، اما میتواند متاستاز دهد (بهویژه به کبد).
- ویژگی کلیدی: اغلب جهش در ژن KIT یا PDGFRA دارند، درمان هدفمند با داروهایی مانند imatinib (Gleevec) بسیار مؤثر است.
- پیشآگهی خوب اگر زود تشخیص داده شود و جراحی + درمان هدفمند انجام گیرد.
۳. لنفوم معده
- حدود ۳–۵٪ موارد سرطان معده.
- سرطان سیستم لنفاوی (معمولاً لنفوم غیرهوچکین).
- شایعترین زیرنوع: MALT lymphoma (Mucosa-Associated Lymphoid Tissue) که اغلب با عفونت هلیکوباکتر پیلوری مرتبط است.
- اگر زود تشخیص داده شود و هلیکوباکتر درمان شود، بسیاری موارد MALT با آنتیبیوتیک به تنهایی بهبود مییابند (بدون نیاز به شیمیدرمانی یا جراحی).
- انواع دیگر: Diffuse large B-cell lymphoma (DLBCL) که تهاجمیتر است و نیاز به شیمیدرمانی/ایمونوتراپی دارد.
- پیشآگهی اغلب بهتر از آدنوکارسینوم است.
۴. تومورهای نورواندوکرین (Neuroendocrine Tumors – NETs) شامل کارسینوئید
- نادر (کمتر از ۵٪).
- از سلولهای نورواندوکرین (سلولهایی که هورمون ترشح میکنند) شروع میشود.
- اغلب کارسینوئید (Carcinoid tumors) نامیده میشوند.
- رشد آهسته، ممکن است هورمون ترشح کنند (سندرم کارسینوئید با علائم flushing، اسهال).
- درجهبندی: G1/G2 (کمتهاجم) یا G3 (نورواندوکرین کارسینومای پرتهاجم).
- درمان: جراحی، درمان هدفمند (somatostatin analogs مانند octreotide)، یا شیمیدرمانی در موارد پیشرفته.
۵. انواع بسیار نادر دیگر
- سرطان سلول سنگفرشی (Squamous cell carcinoma): بسیار نادر، از سلولهای سنگفرشی (شبیه پوست) شروع میشود.
- تومورهای مخلوط یا هیبرید: ترکیب آدنوکارسینوم با NET یا GIST.
- سرطانهای متاستاتیک به معده (از سایر اندامها).
عوامل خطر و علل ابتلا به سرطان معده

سرطان معده (بهویژه نوع آدنوکارسینوم) معمولاً نتیجه ترکیبی از عوامل ژنتیکی، محیطی، عفونی و سبک زندگی است. هیچ علت واحدی وجود ندارد، اما عفونت مزمن هلیکوباکتر پیلوری قویترین و شایعترین عامل شناختهشده است که حدود ۷۵–۹۰٪ موارد سرطان معده غیرکاردیا (بدن و آنتروم معده) را به آن نسبت میدهند. این عوامل خطر را میتوان به دو دسته قابل تغییر (قابل پیشگیری) و غیرقابل تغییر تقسیم کرد.
عوامل خطر اصلی و علل
عفونت هلیکوباکتر پیلوری (H. pylori)
- قویترین عامل خطر شناختهشده (عامل اصلی در بیش از ۷۶٪ موارد جهانی و ایران).
- باعث التهاب مزمن (گاستریت)، آتروفی مخاط، متاپلازی رودهای و در نهایت سرطان میشود.
- درمان (اریکاسیون) با آنتیبیوتیک خطر را بهطور قابل توجهی کاهش میدهد (تا ۴۵–۶۸٪ در بلندمدت).
- در ایران شیوع بالای این باکتری (بهویژه در مناطق روستایی و با بهداشت پایین) یکی از دلایل اصلی شیوع بالا است.
رژیم غذایی نامناسب
- مصرف بالای نمک، غذاهای نمکسود، دودی، فرآوریشده (مانند گوشتهای نمکی، ترشیجات زیاد، فستفود).
- کمبود میوه و سبزیجات تازه (کمبود آنتیاکسیدانها و ویتامین C).
- مصرف غذاهای حاوی نیترات/نیتریت (در برخی گوشتهای فرآوریشده).
- رژیم پرنمک و دودی در ایران و شرق آسیا نقش کلیدی دارد.
سیگار کشیدن و مصرف تنباکو
- خطر را تقریباً دو برابر میکند (۱۵–۲۰٪ موارد مرتبط با سیگار).
- مواد سرطانزا مستقیماً به مخاط معده آسیب میرساند.
- در ایران مصرف سیگار و تریاک/مواد افیونی عامل خطر اضافی است.
مصرف الکل
- مصرف سنگین (بیش از ۳ واحد در روز) خطر را افزایش میدهد، بهویژه برای سرطان کاردیا (بالای معده).
چاقی و اضافه وزن
- خطر سرطان کاردیا و GEJ (اتصال معده-مری) را افزایش میدهد (به دلیل رفلاکس مزمن و التهاب).
- در جهان و ایران در حال افزایش به دلیل سبک زندگی مدرن.
سابقه پزشکی و بیماریهای پیشسرطانی
- گاستریت آتروفیک مزمن، متاپلازی رودهای، دیسپلازی.
- کمخونی پرنیسیوز (کمبود ویتامین B12).
- پولیپ معده (بهویژه آدنوماتوز).
- جراحی قبلی معده (مانند گاسترکتومی برای زخم).
- رفلاکس معده به مری (GERD) مزمن.
- عوامل ژنتیکی و خانوادگی
- سابقه خانوادگی سرطان معده (بهویژه نوع منتشر).
- سندرمهای ارثی نادر مانند:
- جهش CDH1 (سرطان معده منتشر ارثی).
- Lynch syndrome، FAP، Peutz-Jeghers.
- گروه خونی A (خطر کمی بالاتر).
عوامل دیگر
- سن بالا (بیش از ۶۰ سال؛ میانگین تشخیص حدود ۶۸ سال جهانی، اما در ایران گاهی پایینتر).
- جنسیت مرد (تقریباً دو برابر زنان).
- نژاد/منطقه جغرافیایی (بالاتر در آسیای شرقی، آمریکای لاتین، ایران).
- مواجهه شغلی با گرد و غبار، مواد شیمیایی یا پرتودرمانی قبلی.
نقش عفونت هلیکوباکتر پیلوری در ایجاد سرطان معده
هلیکوباکتر پیلوری (H. pylori) یک باکتری مارپیچیشکل است که تقریباً نیمی از جمعیت جهان (حدود ۴٫۴ میلیارد نفر) را آلوده میکند. این باکتری توسط سازمان بهداشت جهانی (WHO) و آژانس بینالمللی تحقیقات سرطان (IARC) به عنوان عامل کلاس I کارسینوژن (سرطانزای قطعی انسانی) طبقهبندی شده و قویترین عامل خطر شناختهشده برای سرطان معده (بهویژه نوع غیرکاردیا در بدن و آنتروم معده) است.
آمار و اهمیت جهانی
- عفونت مزمن هلیکوباکتر مسئول ۷۶٪ از موارد سرطان معده در جهان است.
- بدون تغییر در سیاستهای فعلی، تا پایان عمر افراد متولد ۲۰۰۸–۲۰۱۷، حدود ۱۵٫۶ میلیون مورد جدید سرطان معده پیشبینی میشود که ۱۱٫۹ میلیون (۷۶٪) آن قابل پیشگیری با درمان عفونت است.
- در آسیا (بهویژه شرق آسیا و ایران) بیشترین بار (حدود ۶۷٪ موارد قابلانتساب) وجود دارد.
- در ایران، شیوع بالای این باکتری (بهویژه در مناطق با بهداشت پایینتر) یکی از دلایل اصلی رتبه بالای سرطان معده (اول یا دوم در مردان) است.
مکانیسمهای ایجاد سرطان (پاتوژنز)
هلیکوباکتر مستقیماً سرطان ایجاد نمیکند، بلکه از طریق یک فرآیند چندمرحلهای طولانیمدت (معمولاً ۲۰–۴۰ سال) مخاط معده را تغییر میدهد. این فرآیند بر اساس کاسکاد کورئ توصیف میشود:
- عفونت اولیه و التهاب حاد مزمن
باکتری با تولید اورهآز محیط اسیدی معده را خنثی کرده و در مخاط نفوذ میکند. باعث گاستریت مزمن فعال میشود. - گاستریت آتروفیک
التهاب طولانیمدت باعث از بین رفتن غدد معده (آتروفی) و کاهش ترشح اسید میشود. - متاپلازی رودهای
سلولهای معده به سلولهای شبیه روده تغییر شکل میدهند (پیشسرطانی). - دیسپلازی
تغییرات سلولی پیشسرطانی شدیدتر. - سرطان معده (آدنوکارسینوم)
بهویژه نوع رودهای که با التهاب مزمن مرتبط است.
عوامل کلیدی باکتریایی (ویرولانس فاکتورها)
- CagA (مهمترین پروتئین): از طریق سیستم ترشح نوع IV (T4SS) وارد سلولهای میزبان شده، مسیرهای سیگنالینگ را مختل میکند (مانند NF-κB، Wnt/β-catenin، PI3K/AKT، STAT3، MAPK). باعث التهاب، آسیب DNA، تکثیر غیرطبیعی سلول، از دست رفتن قطبیت سلولی و تبدیل بدخیم میشود.
- VacA (سیتوکسین خلأزا): باعث ایجاد خلأ در سلولها، آپوپتوز، آسیب DNA و التهاب مزمن.
- سایر فاکتورها: BabA، SabA، urease، که چسبندگی و بقا را افزایش میدهند.
- سویههای CagA-positive خطر سرطان را ۲–۴ برابر بیشتر میکنند.
عوامل میزبانی و محیطی
- ژنتیک میزبان (مثل پلیمورفیسمهای IL-1β، TNF-α) التهاب را تشدید میکند.
- رژیم پرنمک، سیگار، کمبود میوه/سبزیجات التهاب را افزایش و حفاظت را کاهش میدهد.
- میکروبیوم معده تغییر یافته (dysbiosis) نقش کمکی دارد.
علائم و نشانههای سرطان معده در مراحل اولیه
سرطان معده (گاستریک کانسر) در مراحل اولیه (مرحله ۰ تا I) اغلب بدون علامت یا با علائم بسیار مبهم و غیراختصاصی است. این علائم معمولاً شبیه به مشکلات گوارشی رایج مانند سوءهاضمه، زخم معده، گاستریت یا رفلاکس هستند، به همین دلیل بسیاری از افراد آنها را نادیده میگیرند یا به عنوان مشکلات ساده تلقی میکنند. این یکی از دلایل اصلی تشخیص دیرهنگام سرطان معده (بهویژه در ایران و کشورهای بدون برنامه غربالگری گسترده) است.
علائم شایع در مراحل اولیه

این علائم اغلب تدریجی ظاهر میشوند و ممکن است ماهها یا سالها ادامه یابند بدون اینکه شدید شوند:
- سوءهاضمه یا ناراحتی مبهم معده : احساس ناراحتی، سنگینی یا فشار در قسمت بالای شکم (اپیگاستر)، اغلب پس از غذا.
- سوزش سر دل یا ترش کردن مداوم : شبیه رفلاکس، اما اگر بیش از چند هفته ادامه یابد و با درمان ساده بهبود نیابد، هشداردهنده است.
- احساس نفخ یا پری زودرس : احساس سیری یا پر بودن معده پس از خوردن مقدار کمی غذا (گاهی بعد از چند لقمه).
- کاهش اشتها : بیمیلی به غذا، حتی غذاهای مورد علاقه، بدون دلیل واضح.
- حالت تهوع خفیف یا مکرر : گاهی همراه با استفراغ خفیف (بدون خون در مراحل اولیه).
- درد یا ناراحتی مبهم در بالای شکم : معمولاً بالای ناف، خفیف و متناوب، نه شدید مانند زخم حاد.
- خستگی یا ضعف عمومی : گاهی به دلیل کمخونی خفیف ناشی از خونریزی پنهان.
نکات مهم درباره علائم اولیه
- این علائم در بیش از ۷۰–۸۰٪ موارد اولیه غیراختصاصی هستند و اغلب با بیماریهای خوشخیم اشتباه گرفته میشوند.
- کاهش وزن غیرمنتظره معمولاً در مراحل اولیه کمتر دیده میشود، اما اگر همراه با علائم بالا باشد، بسیار هشداردهنده است (اغلب در مراحل II به بعد ظاهر میشود).
- در ایران، به دلیل شیوع بالای هلیکوباکتر پیلوری و گاستریت مزمن، این علائم رایجتر هستند و افراد اغلب آنها را به “معده درد عصبی” یا “زخم” نسبت میدهند.
- علائم هشدار قرمز که حتی در مراحل نسبتاً اولیه باید فوری بررسی شوند: ادامهدار بودن بیش از ۲–۴ هفته، عدم بهبود با داروهای معمولی (مانند آنتیاسیدها)، همراهی با کمخونی، مدفوع تیره یا استفراغ خونی (هرچند اینها بیشتر پیشرفته هستند).
علائم هشداردهنده و علائم پیشرفته سرطان معده
سرطان معده اغلب در مراحل اولیه علائم مبهم دارد، اما با پیشرفت بیماری (معمولاً مراحل II تا IV)، علائم هشداردهنده ظاهر میشوند که نشاندهنده نیاز فوری به بررسی پزشکی (مانند آندوسکوپی) هستند. این علائم معمولاً شدیدتر، مداوم و همراه با تغییرات قابل توجه در بدن هستند. تشخیص در این مرحله اغلب دیرهنگام است و پیشآگهی را بدتر میکند.
علائم هشداردهنده (Red Flags) – که حتی اگر خفیف باشند، باید جدی گرفته شوند
این علائم اغلب در مراحل نسبتاً اولیه تا متوسط ظاهر میشوند، اما اگر بیش از ۲–۴ هفته ادامه یابند یا با هم ترکیب شوند، بسیار مشکوک هستند:
- کاهش وزن غیرمنتظره و قابل توجه : بیش از ۵–۱۰٪ وزن بدن در چند ماه بدون رژیم یا ورزش (شایعترین علامت هشداردهنده و پیشآگهی بد).
- کمخونی (آنمی) بدون دلیل واضح: خستگی شدید، رنگپریدگی، تنگی نفس، سرگیجه (اغلب ناشی از خونریزی پنهان مزمن در معده).
- مدفوع سیاهرنگ یا قیری: نشاندهنده خونریزی گوارشی فوقانی (خون هضمشده).
- استفراغ خونی : استفراغ قرمز روشن یا شبیه قهوهای
- درد شدید یا مداوم در قسمت بالای شکم : که با غذا بدتر میشود یا با داروهای معمولی (آنتیاسید، PPI) بهبود نمییابد.
- مشکل در بلع: بهویژه اگر تومور در کاردیا یا بالای معده باشد؛ ابتدا با غذاهای جامد، سپس مایعات.
- تورم یا بزرگ شدن شکم : ناشی از آسیت (آب آوردن شکم) در موارد درگیری صفاق یا کبد.
علائم پیشرفته (مراحل III–IV یا متاستاتیک)
در مراحل پیشرفته، سرطان اغلب به غدد لنفاوی، کبد، صفاق، ریه یا استخوان گسترش یافته و علائم سیستمیک و شدید ایجاد میکند:
- کاهش وزن شدید و لاغری مفرط : همراه با ضعف عمومی و از دست دادن عضلات.
- تهوع و استفراغ مکرر : گاهی خونی یا غیرقابل کنترل.
- درد شدید شکمی مداوم : که ممکن است به پشت یا شانه انتشار یابد.
- تورم شکم و آسیت : شکم بادکرده و سفت به دلیل مایع در صفاق.
- زردی پوست و چشم : اگر سرطان به کبد متاستاز دهد یا مجرای صفراوی را مسدود کند؛ همراه با ادرار تیره و مدفوع کمرنگ.
- خستگی شدید و ضعف عمومی : اغلب به دلیل کمخونی، سوءتغذیه یا متاستاز.
- تورم غدد لنفاوی : بهویژه گره ویرشو در گردن سمت چپ (نشانه کلاسیک متاستاز).
- یبوست یا اسهال شدید، احساس انسداد روده، یا تنگی نفس (اگر متاستاز به ریه باشد).
چه زمانی باید به پزشک مراجعه کرد؟
سرطان معده اغلب در مراحل اولیه علائم مبهم دارد و بسیاری از افراد آنها را نادیده میگیرند یا به مشکلات ساده گوارشی نسبت میدهند. اما تشخیص زودهنگام میتواند تفاوت بزرگی در درمان و پیشآگهی ایجاد کند. زمان مراجعه به پزشک به شرح زیر است:
موارد فوری – همین امروز یا در اسرع وقت به اورژانس یا متخصص مراجعه کنید
- استفراغ خونی (قرمز روشن یا شبیه دانه قهوه) یا مدفوع سیاهرنگ قیری – نشاندهنده خونریزی فعال گوارشی.
- درد شدید و ناگهانی شکم همراه با تب، استفراغ شدید یا عدم توانایی خوردن/نوشیدن.
- تورم ناگهانی شکم (آسیت) یا زردی پوست/چشم – نشانههای احتمالی متاستاز پیشرفته.
- مشکل شدید در بلع که غذا گیر میکند یا بلع مایعات هم سخت است.
موارد هشداردهنده – ظرف ۱–۲ هفته به متخصص گوارش مراجعه کنید (ترجیحاً با آندوسکوپی)
این علائم اگر بیش از ۲–۴ هفته ادامه یابند یا شدید شوند، نیاز به بررسی فوری دارند (حتی اگر خفیف به نظر برسند):
- کاهش وزن غیرمنتظره (بیش از ۵–۱۰٪ وزن بدن در چند ماه بدون رژیم یا ورزش) – شایعترین و مهمترین علامت هشدار.
- کمخونی بدون دلیل (خستگی شدید، رنگپریدگی، تنگی نفس، سرگیجه) – اغلب ناشی از خونریزی پنهان.
- درد یا ناراحتی مداوم بالای شکم که با داروهای معمولی (مانند آنتیاسید یا PPI) بهبود نمییابد.
- سیری زودرس (احساس پر شدن معده پس از مقدار کمی غذا) همراه با کاهش اشتها.
- تهوع یا استفراغ مکرر بدون دلیل واضح.
- تورم یا توده قابل لمس در شکم.
راهنمای سنی و عوامل خطر (برای تصمیمگیری بهتر)
- بالای ۵۵–۶۰ سال (یا بالای ۵۰ سال در ایران/آسیا): اگر علائم جدید سوءهاضمه، سوزش سر دل یا درد معده بیش از ۲–۳ هفته ادامه یابد، حتی بدون علائم شدید، آندوسکوپی توصیه میشود (به دلیل شیوع بالاتر سرطان معده در این سنین و مناطق).
- زیر ۵۰–۵۵ سال: اگر علائم هشداردهنده (مانند کاهش وزن + کمخونی) دارید یا سابقه خانوادگی سرطان معده، عفونت هلیکوباکتر مزمن، سیگار سنگین یا رژیم پرنمک دارید، زودتر مراجعه کنید.
- در ایران: به دلیل شیوع بالای هلیکوباکتر پیلوری و تشخیص دیرهنگام (بیش از ۷۰–۸۰٪ موارد پیشرفته)، اگر علائم بیش از ۲–۳ هفته ادامه یافت یا با درمان ساده (مانند امپرازول) بهتر نشد، به متخصص گوارش مراجعه کنید – آندوسکوپی ساده و ارزان میتواند نجاتدهنده باشد.
روشهای تشخیص سرطان معده
تشخیص سرطان معده (گاستریک کانسر) معمولاً با ترکیبی از تاریخچه بالینی، معاینه فیزیکی و آزمایشهای تخصصی انجام میشود. هدف اصلی، تأیید وجود سرطان، تعیین نوع (مانند آدنوکارسینوم)، مرحله و بررسی گسترش (متاستاز) به سایر اندامهاست. روشهای اصلی به ترتیب اهمیت عبارتند از:
۱. آندوسکوپی فوقانی
- روش اصلی و طلایی برای تشخیص اولیه.
- لوله نازک انعطافپذیر (آندوسکوپ) با دوربین و نور از دهان وارد مری، معده و ابتدای روده کوچک میشود.
- پزشک پوشش داخلی معده را مستقیم مشاهده میکند و هر ناحیه مشکوک (زخم، توده، التهاب غیرطبیعی) را میبیند.
- همزمان بیوپسی (نمونهبرداری) از چندین نقطه انجام میشود (حتی اگر ظاهر طبیعی به نظر برسد، در موارد مشکوک).
- حساسیت بالا (بیش از ۹۵٪ برای تشخیص تومورهای قابل مشاهده).
- در ایران رایجترین روش اولیه است و اغلب سرپایی انجام میشود.
۲. بیوپسی و بررسی پاتولوژیک
- تنها روش قطعی برای تأیید سرطان (نه فقط مشکوک بودن).
- نمونههای کوچک بافت (معمولاً ۶–۱۰ قطعه از نواحی مختلف) طی آندوسکوپی برداشته میشود.
- زیر میکروسکوپ بررسی میشود تا نوع سرطان (رودهای/منتشر، درجه، زیرگروه مانند signet-ring cell)، و تستهای مولکولی (HER2، PD-L1، MSI، EBV، NTRK و غیره) انجام شود.
- بر اساس NCCN 2026، تست بیومارکرها (مانند HER2، MSI-high، PD-L1) برای انتخاب درمان هدفمند/ایمونوتراپی ضروری است.
۳. تصویربرداری برای مرحلهبندی
- سیتیاسکن (CT scan) قفسه سینه، شکم و لگن با کنتراست خوراکی و وریدی: روش استاندارد اولیه برای ارزیابی گسترش موضعی، غدد لنفاوی و متاستاز دور (کبد، ریه، صفاق).
- PET-CT (FDG-PET/CT): توصیهشده برای موارد locally advanced یا metastatic (NCCN 2026). حساسیت بالا برای تشخیص متاستاز پنهان و ارزیابی پاسخ به درمان.
- سونوگرافی آندوسکوپیک (Endoscopic Ultrasound – EUS): برای مرحلهبندی دقیق T (عمق نفوذ تومور در دیواره معده) و N (غدد لنفاوی نزدیک). دقت بالا در تعیین T1–T3 و N.
- MRI: کمتر رایج، اما در موارد خاص (مانند ارزیابی کبد یا صفاق) مفید است.
- لاپاراسکوپی تشخیصی (Diagnostic Laparoscopy): در موارد locally advanced یا مشکوک به متاستاز صفاقی (peritoneal carcinomatosis) توصیه میشود. امکان بیوپسی صفاق و بررسی مایع آسیت.
۴. آزمایشهای آزمایشگاهی کمکی
- CBC (شمارش کامل خون): بررسی کمخونی (شایع به دلیل خونریزی پنهان).
- آزمایشهای عملکرد کبد و کلیه: برای ارزیابی وضعیت کلی و متاستاز کبدی.
- تومور مارکرها (CEA، CA 19-9، CA 72-4): ممکن است افزایش یابند، اما حساسیت/اختصاصیت پایین دارند و بیشتر برای پیگیری استفاده میشوند (نه تشخیص اولیه).
- تست هلیکوباکتر پیلوری: اگر عفونت فعال باشد (برای درمان و کاهش خطر عود).
اهمیت تشخیص زودهنگام
تشخیص زودهنگام سرطان معده (گاستریک کانسر) یکی از مهمترین عوامل تعیینکننده در بهبود پیشآگهی، افزایش شانس درمان موفق و کاهش مرگومیر است. این سرطان اغلب در مراحل اولیه علائم واضحی ندارد و بسیاری از موارد در مراحل پیشرفته تشخیص داده میشوند، که منجر به پیشآگهی ضعیف میشود. اما اگر در مراحل اولیه (localized یا مرحله ۰–I) شناسایی شود، درمان (معمولاً جراحی) بسیار مؤثرتر است و نرخ بقا بهطور چشمگیری افزایش مییابد.
آمار نرخ بقای ۵ ساله بر اساس مرحله
- مرحله localized (محدود به معده، بدون گسترش): حدود ۷۶–۷۷٪ (برخی منابع تا ۷۵–۹۰٪ در کشورهای با غربالگری مانند ژاپن و کره).
- مرحله regional (گسترش به غدد لنفاوی نزدیک): حدود ۳۷٪.
- مرحله distant (متاستاتیک، گسترش دور): تنها ۷–۸٪.
- کل موارد (همه مراحل ترکیبشده): حدود ۳۸٪ (در آمریکا؛ در جهان و ایران پایینتر به دلیل تشخیص دیرهنگام).
این تفاوت چشمگیر (از بیش از ۷۵٪ در مراحل اولیه تا کمتر از ۱۰٪ در پیشرفته) نشان میدهد که تشخیص زودهنگام میتواند شانس بقا را ۱۰ برابر یا بیشتر افزایش دهد.
مزایای کلیدی تشخیص زودهنگام
- درمان کمتر تهاجمی و مؤثرتر: در مراحل اولیه اغلب جراحی محدود (گاسترکتومی جزئی) کافی است و نیاز به شیمیدرمانی گسترده یا درمانهای سیستمیک کمتر میشود. بیمار کیفیت زندگی بهتری حفظ میکند.
- شانس درمان کامل (cure): در مراحل اولیه، بسیاری بیماران کاملاً درمان میشوند و به زندگی عادی بازمیگردند.
- کاهش هزینههای درمانی: درمان پیشرفته (متاستاتیک) بسیار گرانتر و طولانیتر است.
- کاهش مرگومیر: در کشورهایی مانند ژاپن و کره جنوبی که برنامه غربالگری گسترده (آندوسکوپی منظم از ۴۰ سالگی) دارند، نرخ بقا بسیار بالاتر (بیش از ۷۰–۹۰٪ برای موارد تشخیصدادهشده) است، در حالی که در غرب و ایران اغلب کمتر از ۴۰٪ است.
- بهبود کیفیت زندگی: تشخیص زودتر از ایجاد علائم شدید (مانند کاهش وزن شدید، آسیت، زردی) جلوگیری میکند.
وضعیت در ایران
- بیش از ۷۰–۸۰٪ موارد در مراحل پیشرفته تشخیص داده میشوند، که یکی از دلایل اصلی کشنده بودن سرطان معده (رتبه اول یا دوم مرگ سرطانی در مردان) است.
- تأخیر در مراجعه (۳–۶ ماه یا بیشتر) شایع است و میتواند شانس بقای ۵ ساله را از بیش از ۶۰٪ به کمتر از ۵۰٪ کاهش دهد.
- تشخیص زودهنگام میتواند شانس بقا را بهطور معناداری افزایش دهد، اما برنامه غربالگری گسترده وجود ندارد (فقط برای گروههای پرخطر توصیه میشود).
روشهای درمان سرطان معده
درمان سرطان معده (گاستریک کانسر) بر اساس مرحله بیماری، محل تومور (کاردیا، بدن، آنتروم)، نوع هیستولوژیک (رودهای یا منتشر)، وضعیت عملکرد بیمار (PS)، بیومارکرها (HER2، PD-L1، MSI، NTRK و غیره) و وضعیت کلی بیمار تعیین میشود. رویکرد اغلب چندوجهی است و شامل ترکیبی از جراحی، شیمیدرمانی، پرتودرمانی، درمان هدفمند و ایمونوتراپی میگردد. روشهای اصلی درمان به شرح زیر است:
۱. جراحی (Surgery) – پایه درمان curative
- گاسترکتومی جزئی (Subtotal/Partial Gastrectomy): برای تومورهای محدود به آنتروم یا بدن پایین (Distal)، با لنفادنکتومی D2 (استاندارد در آسیا و توصیهشده در غرب).
- گاسترکتومی کامل (Total Gastrectomy): برای تومورهای منتشر، proximal یا منتشر (Diffuse/signet-ring cell).
- گاسترکتومی پروگزیمال (Proximal Gastrectomy): برای تومورهای کاردیا/GEJ.
- لنفادنکتومی D1+ یا D2: استاندارد برای مرحله I–III (بهبود بقا).
- جراحی کمتهاجمی (Laparoscopic/Robotic): در مراکز پیشرفته برای مرحله اولیه، با نتایج مشابه باز.
- هیپرکتومی + HIPEC یا CRS + HIPEC (Cytoreductive Surgery + Hyperthermic Intraperitoneal Chemotherapy): در موارد محدود peritoneal-only disease (NCCN category 2B).
۲. درمان نئوادجوانت/پریاپراتیو (Perioperative/Neoadjuvant Therapy)
- برای مرحله IB–III (resectable locally advanced): شیمیدرمانی perioperative بهترین گزینه.
- رژیمهای ترجیحی (NCCN 2026):
- FLOT (Fluorouracil + Leucovorin + Oxaliplatin + Docetaxel) – استاندارد.
- FLOT + durvalumab (برای PD-L1 CPS ≥1 یا TAP ≥1) – category 1 preferred جدید.
- Fluoropyrimidine + Oxaliplatin + tislelizumab (برای HER2-negative).
- پس از جراحی: ادامه همان رژیم (adjuvant) اگر پاسخ خوب نباشد.
۳. شیمیدرمانی (Chemotherapy)
- Adjuvant (پس از جراحی): برای مرحله II–III، FLOT یا CAPOX (Capecitabine + Oxaliplatin) یا S-1 (در آسیا).
- اولین خط متاستاتیک (First-line metastatic):
- HER2-positive: Chemotherapy (FOLFOX/CAPOX) + Trastuzumab ± Pertuzumab.
- HER2-negative: Chemotherapy + Immunotherapy (Nivolumab یا Pembrolizumab برای PD-L1 CPS ≥5، یا tislelizumab).
- رژیم پایه: FOLFOX، CAPOX، FLOT یا cisplatin-based.
- دومین خط و بعدی: Ramucirumab + Paclitaxel، Irinotecan، TAS-102، trifluridine-tipiracil و غیره.
۴. پرتودرمانی (Radiation Therapy / Radiotherapy)
- اغلب Chemoradiation (شیمی + پرتو) برای مرحله locally advanced unresectable یا پس از جراحی ناکافی (R1/R2 resection).
- رژیم: ۴۵–۵۰.۴ Gy + شیمیدرمانی همزمان (۵-FU یا capecitabine).
- در GEJ/cardia tumors: neoadjuvant chemoradiation (مانند CROSS regimen) گاهی استفاده میشود.
۵. درمان هدفمند (Targeted Therapy)
- HER2-positive (≈۱۵–۲۰٪): Trastuzumab + chemotherapy (اولین خط)؛ T-DXd (Enhertu) در خطوط بعدی.
- NTRK fusion-positive (نادر): Larotrectinib، Entrectinib یا Repotrectinib (category 2A/B).
- VEGF inhibitors: Ramucirumab (دومین خط با paclitaxel).
- سایر: Claudin 18.2-targeted (zolbetuximab در برخی مطالعات جدید).
۶. ایمونوتراپی (Immunotherapy)
- اولین خط: Nivolumab یا Pembrolizumab + chemotherapy برای PD-L1 بالا (CPS ≥5 یا ≥1 در برخی رژیمها).
- Durvalumab + FLOT perioperative جدید اضافه شده.
- دومین خط: Pembrolizumab برای MSI-high/dMMR (≈۵–۱۰٪ موارد).
۷. درمانهای پیشرفته یا پالیاتیو
- برای metastatic/unresectable: Systemic therapy + supportive care (تغذیه، کنترل درد، استنت برای انسداد).
- Palliative surgery: Bypass یا استنت برای انسداد.
- Best supportive care در بیماران با PS ضعیف.
عوارض درمان و مدیریت آنها
درمان سرطان معده (جراحی، شیمیدرمانی، پرتودرمانی، درمان هدفمند و ایمونوتراپی) اغلب مؤثر است، اما میتواند عوارض جانبی کوتاهمدت یا بلندمدت ایجاد کند. این عوارض بسته به نوع درمان، مرحله بیماری، سن، وضعیت کلی بیمار و رژیم درمانی متفاوت هستند. بیشتر عوارض قابل مدیریت یا پیشگیری هستند و با مراقبتهای حمایتی بهبود مییابند.عوارض اصلی و راههای مدیریت آنها به شرح زیر است:
۱. عوارض جراحی (گاسترکتومی جزئی یا کامل)
جراحی اصلیترین درمان curative است، اما میتواند عوارض زیر را ایجاد کند:
- سوءتغذیه و کمبود ویتامینها (شایعترین، بهویژه پس از گاسترکتومی کامل): کمبود ویتامین B12، آهن، کلسیم، ویتامین D → کمخونی، پوکی استخوان، خستگی.
- مدیریت: مکملهای ویتامین B12 (تزریقی ماهانه)، آهن، کلسیم + ویتامین D؛ رژیم غذایی کوچک و مکرر (۵–۶ وعده کوچک)؛ مشاوره تغذیهای منظم؛ گاهی آنزیمهای گوارشی.
- رفلاکس صفرا یا اسید، Dumping syndrome (اسهال، تعریق، سرگیجه پس از غذا)، احساس پری زودرس.
- مدیریت: خوردن آهسته، اجتناب از قندهای ساده، دراز نکشیدن بلافاصله پس از غذا؛ داروهای ضداسید یا پروکینتیک.
- عفونت محل جراحی، نشت آناستوموز (نشت محل اتصال)، لخته خون، مشکلات تنفسی.
- مدیریت: آنتیبیوتیک پیشگیرانه، فیزیوتراپی تنفسی، داروهای ضدلخته؛ پایش دقیق پس از عمل.
- درد مزمن یا مشکلات گوارشی بلندمدت (مانند گاستریت یا انسداد).
- مدیریت: کنترل درد با دارو، پیگیری منظم.
۲. عوارض شیمیدرمانی (FLOT، CAPOX، FOLFOX و غیره)
شایعترین عوارض (اغلب کوتاهمدت، اما برخی ماندگار):
- تهوع و استفراغ (شایعترین): اغلب با داروهای جدید کمتر شدید است.
- مدیریت: داروهای ضدتهوع قوی (مانند ondansetron، aprepitant، dexamethasone) قبل و بعد درمان؛ خوردن غذاهای سبک و سرد؛ زنجبیل یا طب سوزنی کمکی.
- خستگی شدید و ضعف (Fatigue): در اکثر بیماران.
- مدیریت: فعالیت سبک (پیادهروی)، خواب کافی، تغذیه مناسب، گاهی داروهای محرک (مانند methylphenidate در موارد شدید).
- کاهش اشتها، کاهش وزن، زخم دهان (موکوزیت)، تغییر طعم غذا.
- مدیریت: رژیم پرپروتئین/پرکالری، مکملهای غذایی (Ensure یا مشابه)؛ شستشوی دهان با آبنمک یا بیکربنات؛ داروهای موضعی برای زخم دهان.
- اسهال یا یبوست، نوروپاتی (بیحسی دست/پا با oxaliplatin).
- مدیریت: لوپرامید برای اسهال؛ ملین برای یبوست؛ کاهش دوز یا داروهای neuroprotective برای نوروپاتی.
- کاهش گلبولهای سفید (نوتروپنی → عفونت)، کمخونی، کاهش پلاکت (خونریزی/کبودی).
- مدیریت: آزمایش خون منظم؛ G-CSF (مانند filgrastim) برای نوتروپنی؛ تزریق خون یا پلاکت در موارد شدید؛ اجتناب از افراد بیمار.
- ریزش مو (معمولاً موقت).
- مدیریت: کلاه سرد (اگر در دسترس)، روسری یا ویگ.
۳. عوارض پرتودرمانی (Chemoradiation)
اغلب همراه شیمیدرمانی برای locally advanced:
- خستگی شدید، تهوع، اسهال، مشکلات پوستی (قرمزی، تاول در ناحیه شکم).
- مدیریت: کرمهای مرطوبکننده، داروهای ضدتهوع؛ رژیم BRAT (موز، برنج، سیب، نان تست) برای اسهال؛ استراحت کافی.
- عوارض دیررس (کمتر شایع): آسیب به روده کوچک (انسداد، فیبروز)، مشکلات کلیوی یا قلبی.
- مدیریت: پایش طولانیمدت؛ درمان علامتی.
۴. عوارض درمان هدفمند و ایمونوتراپی
- HER2-targeted (تراستوزوماب، T-DXd): اسهال، مشکلات قلبی، مشکلات چشمی (با برخی داروها).
- مدیریت: اکوکاردیوگرافی منظم؛ قطره چشمی.
- ایمونوتراپی (nivolumab، pembrolizumab): خستگی، راش پوستی، مشکلات تیروئید، کولیت (اسهال شدید).
- مدیریت: کورتیکواستروئید برای عوارض ایمنی؛ پایش هورمونها.
راههای پیشگیری از سرطان معده
سرطان معده یکی از سرطانهای قابل پیشگیری است، زیرا بسیاری از عوامل خطر آن (بهویژه عفونت هلیکوباکتر پیلوری، رژیم غذایی نامناسب و سبک زندگی) قابل کنترل یا تغییر هستند. پیشگیری عمدتاً بر کاهش التهاب مزمن مخاط معده و حذف محرکهای سرطانزا تمرکز دارد. هیچ روش ۱۰۰٪ تضمینی وجود ندارد، اما رعایت این راهها خطر را بهطور قابل توجهی کاهش میدهد (تا ۵۰–۷۰٪ در برخی موارد).
۱. درمان و ریشهکنی عفونت هلیکوباکتر پیلوری (قویترین اقدام پیشگیری)
- عفونت مزمن H. pylori مسئول حدود ۷۶٪ موارد سرطان معده است.
- توصیه کلیدی: در افراد مبتلا (بهویژه با سابقه خانوادگی، گاستریت مزمن، زخم معده یا در مناطق پرشیوع مانند ایران)، آزمایش (تنفسی، مدفوعی یا آندوسکوپی) و درمان کامل با آنتیبیوتیک + مهارکننده اسید (معمولاً ۱۰–۱۴ روز) انجام شود.
- درمان زودهنگام خطر را ۳۰–۶۸٪ کاهش میدهد (بیشتر اگر قبل از تغییرات پیشسرطانی باشد).
- در ایران: به دلیل شیوع بالا (بالای ۵۰–۷۰٪ در برخی مناطق)، غربالگری و درمان در گروههای پرخطر (سابقه خانوادگی، سیگار، علائم گوارشی مزمن) توصیه میشود.
۲. رژیم غذایی سالم و کاهش عوامل خطر غذایی
- مصرف بیشتر میوه و سبزیجات تازه: روزانه حداقل ۴–۵ واحد (رنگارنگ: بروکلی، کلم، هویج، فلفل دلمه، توتها، سبزیجات برگدار). غنی از آنتیاکسیدانها و ویتامین C که مخاط معده را محافظت میکنند.
- غلات کامل و فیبر بالا: نان سبوسدار، برنج قهوهای، جو دوسر.
- کاهش شدید مصرف نمک: کمتر از ۵ گرم در روز (ایرانیها اغلب ۱۰–۱۵ گرم مصرف میکنند). نمک زیاد التهاب را افزایش میدهد.
- اجتناب یا کاهش شدید غذاهای پرخطر:
- غذاهای نمکسود، دودی، فرآوریشده (سوسیس، کالباس، ترشیجات زیاد، ماهی/گوشت دودی).
- گوشت قرمز و فرآوریشده زیاد.
- غذاهای سرخشده یا کبابی بیش از حد.
- مصرف مفید: سیر، پیاز، چای سبز، پروبیوتیکها (ماست، کفیر)، روغن زیتون، ماهیهای چرب (امگا-۳).
۳. ترک سیگار و کاهش مصرف الکل
- سیگار خطر را تقریباً دو برابر میکند (۱۵–۲۰٪ موارد مرتبط).
- ترک کامل سیگار و قلیان ضروری است.
- الکل سنگین (بیش از ۱–۲ واحد در روز) خطر را افزایش میدهد → محدود یا حذف کنید.
۴. حفظ وزن سالم و فعالیت بدنی منظم
- چاقی (بهویژه چاقی شکمی) خطر سرطان کاردیا (بالای معده) را افزایش میدهد.
- BMI ۱۸.۵–۲۴.۹ نگه دارید؛ ورزش متوسط (حداقل ۱۵۰ دقیقه در هفته: پیادهروی سریع، شنا، دوچرخه).
- کاهش وزن تدریجی در افراد چاق خطر را کاهش میدهد.
۵. غربالگری و تشخیص زودهنگام در گروههای پرخطر
- غربالگری عمومی در ایران توصیه نمیشود (شیوع متوسط)، اما در گروههای پرخطر ضروری است:
- سابقه خانوادگی سرطان معده (بهویژه نوع منتشر).
- سندرمهای ارثی (CDH1 mutation).
- سابقه گاستریت آتروفیک، متاپلازی رودهای یا دیسپلازی.
- افراد بالای ۴۰–۵۰ سال با علائم مزمن (سوءهاضمه مقاوم، کاهش وزن).
- روش: آندوسکوپی دورهای (هر ۱–۳ سال) + تست هلیکوباکتر.
- در کشورهای با شیوع بالا (ژاپن، کره): غربالگری از ۴۰ سالگی → بقای بالا.
نکته کلیدی در ایران (۱۴۰۴–۱۴۰۵ / ۲۰۲۵–۲۰۲۶)
- ترکیب هلیکوباکتر + رژیم پرنمک/دودی + سیگار اصلیترین عامل است.
- با دو اقدام ساده (درمان هلیکوباکتر + اصلاح رژیم: میوه/سبزی بیشتر، نمک کمتر) میتوان گام بزرگی برداشت.
- پیشگیری اولیه (سبک زندگی) + ثانویه (غربالگری پرخطر) بیشترین تأثیر را دارد.


Leave Your Comment