جدیدترین درمانهای آرتروز
- 2025-12-10
- 0 Likes
- 0 Comments
مقدمه: آرتروز چیست؟
آرتروز (که در زبان فارسی اغلب به بیماریهای مفصلی التهابی و تخریبی اطلاق میشود) یک اصطلاح عمومی برای مشکلات مفاصل است آرتروز به گروهی از بیماریها اشاره دارد که باعث التهاب، درد و آسیب به مفاصل میشود و امروزه با جدیدترین درمانهای آرتروز قابل ردرمان است.
بیش از ۱۰۰ نوع آرتریت شناخته شده وجود دارد، اما شایعترین آنها استئوآرتریت (که در فارسی اغلب به آن “آرتروز” یا “ساییدگی مفصل” میگویند) و آرتریت روماتوئید است. این بیماریها میلیونها نفر را در جهان تحت تأثیر قرار میدهند و میتوانند کیفیت زندگی را کاهش دهند. در گذشته درمان آرتروز بسیار مشکل بود اما امروزه با جدیدترین درمان های آرتروز قابل درمان است.
انواع آرتروز
استئوآرتریت (OA)
- تعریف: شایعترین نوع آرتروز است که به آن “بیماری ساییدگی و فرسودگی مفاصل” نیز میگویند. در این بیماری، غضروف مفصلی (بافت نرم و محافظ انتهای استخوانها) به تدریج تخریب میشود و استخوانها مستقیماً به هم ساییده میشوند.
- علت اصلی: فرسایش طبیعی با افزایش سن، استفاده بیش از حد از مفصل، چاقی، آسیبهای قبلی یا عوامل ژنتیکی. این بیماری غیرالتهابی است (التهاب ثانویه ایجاد میشود).
- مفاصل شایع: زانو، لگن، دستها، ستون فقرات و شانه.
- ویژگیها: معمولاً در افراد بالای ۵۰ سال شایعتر است و به صورت نامتقارن (یک سمت بدن بیشتر) ظاهر میشود. پیشرفت آن کند است و اغلب با فعالیت بدتر میشود.
آرتریت روماتوئید (Rheumatoid Arthritis – RA)
- تعریف: یک بیماری خودایمنی التهابی مزمن است که در آن سیستم ایمنی بدن به اشتباه به بافتهای سالم مفاصل (به ویژه غشای سینوویال) حمله میکند و باعث التهاب شدید، تورم و آسیب دائمی میشود.
- علت اصلی: ترکیبی از عوامل ژنتیکی، محیطی (مانند سیگار کشیدن) و اختلال ایمنی. التهاب اصلی و اولیه است.
- مفاصل شایع: دستها (به ویژه انگشتان)، مچ، پا و زانو. اغلب متقارن (هر دو سمت بدن) درگیر میشود.
- ویژگیها: میتواند در سنین پایینتر (۳۰ تا ۵۰ سال) شروع شود، علائم آن سریعتر ظاهر میشوند و ممکن است ارگانهای دیگر مانند قلب، ریه یا پوست را نیز درگیر کند. سفتی صبحگاهی طولانی (بیش از یک ساعت) از نشانههای بارز آن است.
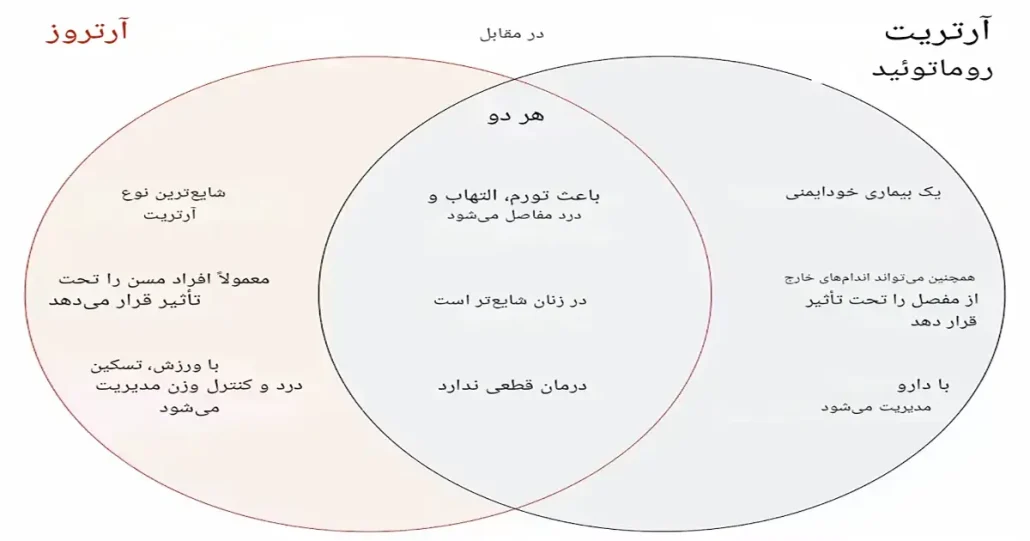
تفاوتهای کلیدی بین استئوآرتریت و آرتریت روماتوئید
| ویژگی | استئوآرتریت (OA) | آرتریت روماتوئید (RA) |
|---|---|---|
| علت | فرسایش مکانیکی و پیری | حمله خودایمنی سیستم ایمنی |
| نوع التهاب | ثانویه و خفیف | اولیه و شدید |
| سن شروع | معمولاً بالای ۵۰ سال | ۳۰ تا ۶۰ سال |
| الگوی درگیری | نامتقارن، مفاصل تحملکننده وزن | متقارن، مفاصل کوچک دست و پا |
| پیشرفت | کند و تدریجی | سریعتر و نوسانی |
| درگیری ارگانها | فقط مفاصل | ممکن است ارگانهای دیگر را درگیر کند |
علائم شایع آرتروز

آرتروز (به ویژه استئوآرتریت و آرتریت روماتوئید) با علائم مشترکی مانند درد، سفتی و تورم مفاصل همراه است، اما شدت، مدت و الگوی آنها متفاوت است. علائم معمولاً به تدریج ظاهر میشوند و با پیشرفت بیماری بدتر میگردند. تشخیص زودهنگام این علائم میتواند به مدیریت بهتر بیماری کمک کند.
علائم مشترک در هر دو نوع آرتروز
- درد مفاصل: اغلب اصلیترین علامت است و میتواند مداوم یا متناوب باشد.
- سفتی مفاصل: به ویژه پس از بیدار شدن از خواب یا دورههای طولانی بیحرکتی.
- تورم و التهاب: مفاصل ممکن است متورم، گرم یا حساس به لمس شوند.
- کاهش دامنه حرکتی: دشواری در خم کردن یا صاف کردن کامل مفصل.
- صدای ساییدگی یا تقتق: هنگام حرکت مفصل (به ویژه در استئوآرتریت).
علائم شایع استئوآرتریت (OA – آرتروز ساییدگی)
این نوع شایعترین آرتروز است و معمولاً با فرسایش غضروف همراه است. علائم اغلب در مفاصل تحملکننده وزن مانند زانو، لگن و ستون فقرات ظاهر میشوند:
- درد که با فعالیت افزایش مییابد و با استراحت کاهش پیدا میکند.
- سفتی صبحگاهی کوتاهمدت (معمولاً کمتر از ۳۰ دقیقه).
- تورم خفیف و احساس ناپایداری مفصل.
- تشکیل زائدههای استخوانی (bone spurs) که ممکن است به صورت برآمدگی سخت احساس شود.
- بدتر شدن علائم با افزایش سن، چاقی یا استفاده بیش از حد از مفصل.
علائم شایع آرتریت روماتوئید (RA – آرتروز التهابی)
این نوع خودایمنی است و اغلب مفاصل کوچک دست، مچ و پا را به صورت متقارن (هر دو سمت بدن) درگیر میکند:
- سفتی صبحگاهی طولانی (بیش از ۱ ساعت) که با حرکت بهبود مییابد.
- تورم شدید، گرمی و قرمزی مفاصل.
- خستگی شدید، تب خفیف، کاهش وزن و ضعف عمومی.
- درگیری ارگانهای دیگر مانند پوست (گرههای روماتوئید)، چشم (خشکی)، ریه یا قلب.
- علائم نوسانی (دورههای تشدید یا flare-up) که ممکن است سریع ظاهر شوند.
جدیدترین درمانهای آرتروز
درمانهای سنتی و رایج (داروهای ضدالتهاب، فیزیوتراپی، کاهش وزن)
درمانهای سنتی و رایج آرتروز (استئوآرتریت و آرتریت روماتوئید) بر پایه کنترل علائم، کاهش التهاب، حفظ عملکرد مفاصل و جلوگیری از پیشرفت بیماری تمرکز دارند. این درمانها اغلب اولین خط درمانی هستند و شامل رویکردهای غیرجراحی و غیرپیشرفته میشوند. هیچکدام درمان قطعی نیستند، اما میتوانند کیفیت زندگی را به طور قابل توجهی بهبود بخشند.
اصول کلی درمانهای سنتی
- رویکرد پلکانی: شروع با درمانهای غیر دارویی (مانند تغییر سبک زندگی)، سپس داروهای ساده و در نهایت درمانهای پیشرفتهتر.
- ترکیبی: اغلب ترکیبی از دارو، فیزیوتراپی و تغییرات سبک زندگی توصیه میشود.
- هدف: کاهش درد، بهبود حرکت و جلوگیری از ناتوانی.
درمانهای رایج برای استئوآرتریت (OA – آرتروز ساییدگی)
این نوع عمدتاً مکانیکی است و درمانها بیشتر علامتی هستند:
- داروهای ضدالتهاب غیراستروئیدی (NSAIDs): مانند ایبوپروفن، ناپروکسن یا دیکلوفناک (خوراکی یا موضعی). قویاً توصیه میشوند، اما با کمترین دوز و کوتاهترین مدت به دلیل عوارض گوارشی و قلبی.
- استامینوفن (پاراستامول): برای درد خفیف، به صورت کوتاهمدت.
- فیزیوتراپی و ورزش: تقویت عضلات اطراف مفصل، بهبود دامنه حرکتی و کاهش درد (مانند ورزشهای آبی یا تایچی).
- کاهش وزن: حتی کاهش ۵-۱۰ کیلوگرم میتواند فشار روی زانو و لگن را تا ۵۰% کاهش دهد.
- وسایل کمکی: عصا، بریس یا کفی کفش برای حمایت از مفاصل.
درمانهای رایج برای آرتریت روماتوئید (RA – آرتروز التهابی)
این نوع خودایمنی است و درمانها اصلاحکننده بیماری هستند تا پیشرفت را متوقف کنند:
- داروهای ضد روماتیسمی اصلاحکننده بیماری معمولی (csDMARDs): متوتریکسات (Methotrexate) اولین انتخاب و استاندارد طلایی است. همراه با هیدروکسیکلروکین یا سولفاسالازین.
- کورتیکواستروئیدها: مانند پردنیزون برای کنترل سریع التهاب (کوتاهمدت).
- NSAIDs و ضدالتهابها: برای کنترل درد و تورم.
- فیزیوتراپی: حفظ حرکت مفاصل و جلوگیری از سفتی.
- کاهش وزن و سبک زندگی: کاهش التهاب سیستمیک و بهبود پاسخ به درمان.
مقایسه درمانهای سنتی در دو نوع آرتروز
| درمان | استئوآرتریت (OA) | آرتریت روماتوئید (RA) |
|---|---|---|
| داروهای اصلی | NSAIDs، استامینوفن، موضعیها | متوتریکسات + NSAIDs، کورتیکواستروئیدها |
| فیزیوتراپی | قویاً توصیهشده (تقویت عضلات) | ضروری (حفظ حرکت و جلوگیری از بدشکلی) |
| کاهش وزن | بسیار مؤثر (کاهش فشار مکانیکی) | مفید (کاهش التهاب سیستمیک) |
| هدف اصلی | کنترل درد و علائم | اصلاح بیماری و جلوگیری از آسیب دائمی |
| جراحی | در موارد پیشرفته (تعویض مفصل) | کمتر، مگر بدشکلی شدید |
این درمانها پایه مدیریت آرتروز هستند و اغلب با موفقیت علائم را کنترل میکنند. همیشه تحت نظر متخصص روماتولوژی شروع شوند تا عوارض کمینه شود.
تزریقهای مفصلی (کورتیکواستروئید، هیالورونیک اسید، PRP)

تزریقهای داخل مفصلی یکی از درمانهای رایج و مؤثر برای کنترل علائم آرتروز (به ویژه استئوآرتریت زانو، لگن و سایر مفاصل) هستند. این روشها معمولاً زمانی استفاده میشوند که درمانهای سنتی مانند داروهای خوراکی، فیزیوتراپی و کاهش وزن کافی نباشند. سه نوع اصلی تزریق شامل کورتیکواستروئیدها، هیالورونیک اسید و پلاسمای غنی از پلاکت (PRP) هستند. این تزریقها اغلب تحت هدایت سونوگرافی یا فلوروسکوپی انجام میشوند تا دقت بالاتر رود. این درمانها علامتی هستند و بیماری را درمان نمیکنند، اما میتوانند درد و عملکرد را بهبود بخشند.
۱. تزریق کورتیکواستروئید (Corticosteroid Injections)
- مکانیسم: کاهش سریع التهاب و درد با مهار پاسخ ایمنی و التهابی.
- کاربرد اصلی: استئوآرتریت (OA) و آرتریت روماتوئید (RA) در دورههای تشدید (flare-up). مؤثر برای درد کوتاهمدت.
- مدت اثر: معمولاً ۴-۸ هفته (سریعالاثر اما کوتاهمدت).
- مزایا: بهبود سریع درد و تورم؛ ارزان و در دسترس.
- معایب و عوارض: تکرار زیاد ممکن است باعث تخریب غضروف، نازک شدن پوست، افزایش قند خون یا عفونت شود. توصیه میشود حداکثر ۳-۴ بار در سال و با فاصله حداقل ۳ ماه.
- شواهد ۲۰۲۵: مؤثر کوتاهمدت، اما در بلندمدت (بیش از ۶ ماه) کمتر از PRP یا HA.
۲. تزریق هیالورونیک اسید (Hyaluronic Acid – Viscosupplementation)
- مکانیسم: جایگزینی مایع سینوویال طبیعی مفصل؛ روانکننده و ضربهگیر، کاهش اصطکاک و التهاب خفیف.
- کاربرد اصلی: عمدتاً استئوآرتریت زانو (درجه متوسط)؛ گاهی لگن یا شانه.
- مدت اثر: ۳-۶ ماه (شروع اثر کندتر، اما طولانیتر از کورتیکواستروئید).
- مزایا: بهبود عملکرد و درد متوسط؛ ممکن است نیاز به تعویض مفصل را به تأخیر بیندازد.
- معایب و عوارض: تورم موقت، هزینه بالاتر؛ در برخی راهنماها (مانند AAOS) توصیه ضعیف دارد.
- شواهد ۲۰۲۵: بهتر از پلاسبو در میانمدت؛ ترکیب با PRP یا کورتیکواستروئید نتایج بهتری میدهد.
۳. تزریق پلاسمای غنی از پلاکت (Platelet-Rich Plasma – PRP)
- مکانیسم: از خون خود بیمار گرفته میشود؛ پلاکتها فاکتورهای رشد آزاد میکنند که التهاب را کاهش، ترمیم بافت و غضروف را تحریک میکنند.
- کاربرد اصلی: استئوآرتریت زانو (درجه خفیف تا متوسط)؛ گزینه احیا کننده.
- مدت اثر: ۶-۱۲ ماه یا بیشتر (بهتر در بلندمدت).
- مزایا: طبیعی، کمعارضه؛ بهبود درد و عملکرد بالینی معنادار؛ غلظت پلاکت بالا (بیش از ۱ میلیون/میکرولیتر) نتایج بهتری دارد.
- معایب و عوارض: هزینه بالا، نیاز به چندین تزریق (۱-۳ بار)؛ نتایج متغیر به دلیل عدم استانداردسازی.
- شواهد ۲۰۲۵: متاآنالیزها نشان میدهند PRP در ۶-۱۲ ماه بهتر از کورتیکواستروئید و اغلب بهتر از HA است؛ بهبود معنادار بالینی در درد و عملکرد.
مقایسه تزریقهای مفصلی در آرتروز
| ویژگی | کورتیکواستروئید | هیالورونیک اسید | PRP |
|---|---|---|---|
| شروع اثر | سریع (۱-۲ هفته) | متوسط (۲-۴ هفته) | متوسط تا کند (۴-۸ هفته) |
| مدت اثر | کوتاه (۴-۸ هفته) | متوسط (۳-۶ ماه) | طولانی (۶-۱۲ ماه یا بیشتر) |
| بهبود درد | عالی کوتاهمدت | خوب متوسط | عالی بلندمدت |
| بهبود عملکرد | خوب کوتاهمدت | خوب متوسط | عالی بلندمدت |
| عوارض | تخریب غضروف با تکرار، عفونت | تورم موقت | کم (درد موقت تزریق) |
| هزینه | پایین | متوسط | بالا |
| توصیه راهنماها | قوی برای کوتاهمدت (ACR/EULAR) | مشروط (برای زانو) | مشروط/در حال افزایش (بهتر از پلاسبو) |
| بهترین برای | تشدید حاد | OA متوسط زانو | OA خفیف-متوسط، بیماران جوانتر |
این تزریقها اغلب ایمن هستند، اما باید توسط متخصص (روماتولوژیست یا ارتوپد) انجام شوند. انتخاب نوع تزریق بستگی به شدت بیماری، سن، مفصل درگیر و پاسخ به درمانهای قبلی دارد. مطالعات اخیر نشان میدهند ترکیب PRP + HA ممکن است بهترین نتایج را بدهد. اگر علائم شدید دارید، با پزشک مشورت کنید تا گزینه مناسب انتخاب شود.
پیشرفتهای دارویی جدید (مهارکنندههای JAK، بیولوژیکها مانند IL-23 inhibitors)
در سالهای اخیر، پیشرفتهای دارویی در درمان آرتروز (به ویژه آرتریت روماتوئید و آرتریت پسوریاتیک) بر پایه داروهای هدفمند تمرکز داشته که سیستم ایمنی را تنظیم میکنند. این داروها disease-modifying (اصلاحکننده بیماری) هستند و نه تنها علائم را کنترل، بلکه پیشرفت آسیب مفصلی را کند میکنند. تا دسامبر ۲۰۲۵، مهارکنندههای JAK (Janus Kinase) و بیولوژیکهای جدید مانند مهارکنندههای IL-23 (اینترلوکین-۲۳) نقش کلیدی ایفا کردهاند. این داروها اغلب برای بیمارانی که به درمانهای سنتی پاسخ ندادهاند، تجویز میشوند. طبق شواهد جدید، جدیدترین درمان های آرتروز کیفیت زندگی را بهبود بخشیده، اما با عوارض احتمالی مانند افزایش ریسک عفونت یا سرطان همراه هستند. همیشه تحت نظارت متخصص روماتولوژی مصرف شوند.
مهارکنندههای JAK: پیشرفتهای جدید در آرتریت روماتوئید (RA)
مهارکنندههای JAK داروهای خوراکی هستند که سیگنالهای التهابی را در سلولها مهار میکنند. این کلاس دارویی از سال ۲۰۱۲ وارد بازار شده و تا ۲۰۲۵، نسلهای جدیدتر با گزینش بالاتر (مانند تمرکز روی JAK1) توسعه یافتهاند. تأیید کرده که جدیدترین درمان های آرتروز باعث بهبود سریع درد و عملکرد مفاصل را فراهم میکنند. پیشرفتهای کلیدی:
- Tofacitinib (Xeljanz): اولین JAK inhibitor، مؤثر در کاهش درد حتی بیشتر از بیولوژیکها در برخی مطالعات.
- Upadacitinib (Rinvoq) و Baricitinib (Olumiant): گزینههای قوی برای آرتریت روماتوئید متوسط تا شدید، با بهبود سریع علائم در ۳ ماه.
- Filgotinib: نسل جدید با گزینش بالا، در ۲۰۲۵ گستردهتر تأیید شده و علائم را به طور معنادار بهبود میبخشد.
- پیشرفتهای ۲۰۲۵: استفاده از ماشین لرنینگ برای پیشبینی پاسخ بیماران، کاهش ریسک سرطان (کمی) با نظارت بهتر. EULAR ۲۰۲۵ بر “JAK It Out” تمرکز کرده و این داروها را برای بیماران مقاوم توصیه میکند.
بیولوژیکها مانند مهارکنندههای IL-23: تمرکز روی آرتریت پسوریاتیک (PsA) و RA
بیولوژیکها پروتئینهای مهندسیشده هستند که سایتوکینهای التهابی را هدف قرار میدهند. مهارکنندههای IL-23 (که التهاب در پوست و مفاصل را کنترل میکنند) بیشتر برای PsA (که اغلب با پسوریازیس همراه است) مؤثرند، اما در RA نیز بررسی میشوند. تا ۲۰۲۵، دادههای بلندمدت نشاندهنده جلوگیری از آسیب ساختاری مفاصل است.
- Guselkumab (Tremfya): تنها IL-23 inhibitor که آسیب مفصلی را به طور قابل توجه مهار میکند؛ دادههای بلندمدت ۲۰۲۵ تأیید کرده.
- Risankizumab (Skyrizi): جدیدتر (در ۵ سال اخیر)، بهبود پوست و مفاصل در PsA؛ برای axial PsA (درگیری ستون فقرات) بحثبرانگیز اما امیدوارکننده.
- پیشرفتهای ۲۰۲۵: ترکیب با TNF inhibitors برای نتایج بهتر؛ کاهش CRP و بهبود MRI در PsA. GRAPPA ۲۰۲۱ و EULAR ۲۰۲۳ این داروها را برای تمام دامنههای PsA (مفاصل، پوست، ناخن) توصیه میکنند. در RA، IL-23 کمتر مستقیم، اما در ترکیب با JAK بررسی میشود.
مقایسه پیشرفتهای دارویی جدید (بر اساس شواهد ۲۰۲۴-۲۰۲۵)
| ویژگی | مهارکنندههای JAK (مانند Filgotinib) | مهارکنندههای IL-23 (مانند Guselkumab) |
|---|---|---|
| کاربرد اصلی | آرتریت روماتوئید متوسط-شدید، مقاوم به متوتریکسات | PsA با درگیری پوست و مفاصل |
| روش مصرف | خوراکی (راحتی بیشتر) | تزریقی (زیرجلدی) |
| شروع اثر | سریع (۲-۴ هفته) | متوسط (۴-۸ هفته) |
| مدت اثر | مداوم با مصرف روزانه | طولانی (هر ۴-۸ هفته) |
| مزایا | بهبود درد سریع، real-world evidence قوی | جلوگیری از آسیب ساختاری، ترکیبپذیری |
| عوارض | ریسک عفونت، سرطان modest | عفونت، سردرد؛ کمتر قلبی |
| توصیه راهنماها | ACR/EULAR: قوی برای آرتریت روماتوئید | GRAPPA/EULAR: قوی برای PsA |
تحریک عصبی واگوس (Vagus Nerve Stimulation) برای کاهش التهاب
تحریک عصبی واگوس (VNS) یکی از جدیدترین درمان های آرتروز در زمینه طب الکترونیکی زیستی (Bioelectronic Medicine) است که التهاب مزمن را بدون نیاز به داروهای سرکوبکننده سیستم ایمنی کنترل میکند. عصب واگوس طولانیترین عصب بدن است که از مغز به ارگانهای مختلف (مانند قلب، ریه و طحال) امتداد دارد و نقش کلیدی در تنظیم پاسخ التهابی دارد. تحریک این عصب مسیر التهابی کولینرژیک را فعال میکند و تولید سایتوکینهای التهابی مانند TNF-α را کاهش میدهد. این روش به ویژه برای بیماریهای التهابی مزمن مانند آرتریت روماتوئید (RA) امیدوارکننده است و تا دسامبر ۲۰۲۵ پیشرفتهای چشمگیری داشته است.
مکانیسم عمل VNS در کاهش التهاب
- عصب واگوس سیگنالهای ضدالتهابی به طحال و سایر ارگانها ارسال میکند.
- تحریک الکتریکی آن باعث آزادسازی استیلکولین میشود که ماکروفاژها را مهار کرده و التهاب را خاموش میکند.
- برخلاف داروهای سنتی، سیستم ایمنی را سرکوب نمیکند و ریسک عفونتهای جدی را کاهش میدهد.
انواع تحریک عصبی واگوس
۱. ایمپلنت (کاشتنی): دستگاه کوچک (اندازه یک ژلهبین) در گردن روی عصب واگوس چپ کاشته میشود و روزانه ۱ دقیقه تحریک میکند.
۲. غیرتهاجمی (Transcutaneous – tVNS یا taVNS): از طریق الکترود روی گوش (شاخه اوريكولار عصب واگوس) انجام میشود؛ بدون جراحی و قابل استفاده در منزل.
کاربرد در آرتریت روماتوئید (RA)
- در سال ۲۰۲۵، FDA دستگاه SetPoint System را برای آرتریت روماتوئید متوسط تا شدید در بیمارانی که به بیولوژیکها یا DMARDهای هدفمند پاسخ ندادهاند یا تحمل نکردهاند، تأیید کرد.
- بر اساس مطالعه pivotal RESET-RA (۲۴۲ بیمار، دوسوکور و کنترلشده با sham):
- کاهش معنادار فعالیت بیماری (DAS28-CRP)، تورم و درد مفاصل.
- جلوگیری از آسیب ساختاری مفاصل در بلندمدت (تا ۱۲-۲۴ ماه).
- نتایج منتشرشده جدیدترین درمان های آرتروز نشاندهنده ایمنی و اثربخشی بالا است.
- مزایا: یکبار کاشت، هزینه کمتر در بلندمدت، عوارض جانبی کمتر (مانند خشکی صدا موقت).
- مناسب برای بیماران مقاوم به درمان دارویی.
کاربرد در استئوآرتریت (OA – آرتروز ساییدگی)
- مطالعات اخیر (۲۰۲۴-۲۰۲۵) روی tVNS غیرتهاجمی تمرکز دارند:
- کاهش درد زانو و دست، بهبود عملکرد و آستانه درد فشاری.
- در مدلهای حیوانی، پیشرفت استئوآرتریت را کند کرده است.
- کارآزماییهای انسانی (مانند ESTIVAL برای دست erosive) بهبود عملکرد نشان داده، اما کاهش درد همیشه معنادار نبوده.
- هنوز FDA تأیید ندارد و بیشتر در مرحله آزمایشی است، اما امیدوارکننده برای التهاب خفیف استئوآرتریت .
مقایسه انواع VNS در درمان آرتروز
| ویژگی | ایمپلنت (SetPoint System) | غیرتهاجمی (tVNS/taVNS) |
|---|---|---|
| کاربرد اصلی | آرتریت روماتوئید مقاوم به دارو | OA زانو/دست، درد مزمن |
| روش | جراحی کاشت در گردن | الکترود روی گوش، روزانه ۲۰-۳۰ دقیقه |
| مدت اثر | بلندمدت (سالها) | کوتاه تا متوسط (نیاز به تکرار) |
| شواهد | قوی (FDA-approved، مطالعات بزرگ) | مقدماتی (کارآزماییهای کوچک) |
| عوارض | جراحی (عفونت نادر)، خشکی صدا موقت | خفیف (سوزش پوست) |
| دسترسی | بیمارستان، تحت نظر متخصص | خانگی، آسانتر |
| بهترین برای | آرتریت روماتوئید شدید و مقاوم | OA خفیف-متوسط، بیماران ترس از جراحی |
این روش انقلابی در درمان التهابی هست و جدیدترین درمان های آرتروز است و ممکن است در آینده برای بیماریهای دیگر مانند کرون، لوپوس یا حتی افسردگی گسترش یابد. با این حال، انتخاب آن بستگی به نوع آرتروز، شدت و پاسخ به درمانهای قبلی دارد. حتماً با متخصص روماتولوژی یا نورولوژیست مشورت کنید تا ارزیابی شود.
درمانهای بازسازی غضروف (ژندرمانی، مهار پروتئینهای پیری، تزریق ژلهای نوین)
درمانهای بازسازی غضروف (Cartilage Regeneration Therapies) یکی از هیجانانگیزترین و جدیدترین درمان های آرتروز در مدیریت آرتروز (به ویژه استئوآرتریت) است. این رویکردها بر خلاف درمانهای سنتی که تنها علائم را کنترل میکنند، بر ترمیم و بازسازی بافت غضروف تمرکز دارند. تا دسامبر ۲۰۲۵، تحقیقات نشاندهنده پیشرفتهای چشمگیری در ژندرمانی، مهارکنندههای پروتئینهای پیری (سنولیتیکها) و تزریق ژلهای نوین (هیدروژلها) است. این روشها اغلب میتوانند آسیب غضروف را معکوس کنند، اما بیشتر در مرحله آزمایشی یا اولیه بالینی قرار دارند. طبق مطالعات اخیر، این درمانها میتوانند ضخامت غضروف را افزایش دهند و پیشرفت بیماری را کند کنند. در ادامه، به جزئیات هر کدام میپردازیم.
ژندرمانی (Gene Therapy)
ژندرمانی با انتقال ژنهای درمانی به سلولهای مفصلی، بیان پروتئینهای مفید را افزایش یا عوامل التهابی را مهار میکند. این روش پتانسیل درمان ریشهای آرتروز را دارد و مزایایی مانند هدفمندی بالا، نیمعمر طولانی و عوارض کم دارد.
- مکانیسم: انتقال ژن محلی به سینوویوم (غشای مفصلی) برای مهار IL-1 (اینترلوکین-۱)، که modulator کلیدی آسیب غضروف است. یا مهندسی سلولهای بنیادی برای تولید غضروف جدید و مبارزه با التهاب.
- پیشرفتهای ۲۰۲۵: مطالعه استنفورد نشان داد مهار تنظیمکننده اصلی پیری (مانند پروتئین ۱۵-PGDH سنسانس) با تزریق مهارکننده (دارو)، غضروف را در مدلهای حیوانی (موشهای پیر) بازسازی میکند و ممکن است به صورت خوراکی یا تزریقی استفاده شود. اثربخشی ژندرمانی را برای استئوآرتریت تأیید کرد، با پتانسیل غیرجراحی. همچنین، ترکیب با نانوتکنولوژی برای پاسخ ایمنی و بازسازی بافت.
- کاربرد: مناسب برای استئوآرتریت ناشی از پیری یا آسیب؛ در مرحله بالینی اولیه، اما امیدوارکننده برای جلوگیری از تعویض مفصل.
- عوارض: ریسک عفونت یا پاسخ ایمنی، اما کمتر از داروهای سنتی.
مهار پروتئینهای پیری (Senescence Protein Inhibitors – Senolytics)
سلولهای سنسسانت (پیری) در استئوآرتریت انباشته میشوند و SASP (فاکتورهای التهابی) تولید میکنند که غضروف را تخریب میکند. سنولیتیکها این سلولها را به طور انتخابی حذف میکنند و التهاب را کاهش میدهند.
- مکانیسم: هدف قرار دادن پروتئینهایی مانند p53 یا ADAM19 در سلولهای سنسسانت chondrocytes (سلولهای غضروفی). این داروها اکسیداتیو استرس را کاهش و بازسازی را تحریک میکنند.
- پیشرفتهای ۲۰۲۵:ترکیب داساتینیب + کوئرستین (سنولیتیک کلاسیک) سلولهای سنسسانت کندروسیتها را کاهش میدهد و استئوآرتریت مفصل فکی را در موشها بهبود میبخشد. پرو داروی SSK1 (هدفگیرنده β-گالاکتوزیداز) استئوآرتریت پیشبالینی را بهبود میبخشد. UBX0101 (مهارکننده p53) به آزمایشهای بالینی رسیده و درد را بدون آسیب بافتی کاهش میدهد. همچنین، کاهش SASP (مانند IL-6) در محیط پیری استئوآرتریت مشاهده شده است.
- کاربرد: برای استئوآرتریت مرتبط با پیری؛ کاهش درد، تورم و آسیب ساختاری.
- عوارض: خفیف، اما نیاز به نظارت برای اثرات سیستمیک.
تزریق ژلهای نوین (Novel Hydrogel Injections)
هیدروژلهای تزریقی محیط سهبعدی مشابه غضروف طبیعی ایجاد میکنند و سلولها، داروها یا فاکتورهای رشد را حمل میکنند تا بازسازی را تحریک کنند. این روش کمتهاجمی است و خواصی مانند خودترمیمی و زیستتخریبپذیری دارد.
- مکانیسم: تزریق مستقیم به مفصل؛ هیدروژلها اصطکاک را کاهش، سلولهای بنیادی را نگه میدارند و التهاب را کنترل میکنند.
- پیشرفتهای ۲۰۲۵: هیدروژل سلولدار با سلولهای بنیادی مزانشیمی برای تعمیر غضروف در خرگوشها. هیدروژل چسبنده با اگزوزومها برای خودترمیمی و زیستسازگاری بالا. هیدروژل بارگذاریشده با دو دارو برای تنظیم ایمنی و تمایز سلولهای غضروفی. هیدروژل هیالورونیک اسید نوترکیب با قدرت مکانیکی بالا برای بازسازی. ترکیب با اورتوبیولوژیکها برای کاهش درد و بازسازی. هیدروژل متقاطعشده با اگزوزوم برای رویکرد نوین بالینی. همچنین، پلیمرهای هیدروژل برای مهندسی غضروف مفصلی.
- کاربرد: استئوآرتریت زانو یا لگن؛ مناسب برای آسیبهای کوچک تا متوسط.
- عوارض: تورم موقت؛ هزینه بالا در مراحل اولیه.
مقایسه درمانهای بازسازی غضروف (بر اساس شواهد ۲۰۲۵)
| ویژگی | ژندرمانی | مهار پروتئینهای پیری (سنولیتیکها) | تزریق ژلهای نوین (هیدروژلها) |
|---|---|---|---|
| مکانیسم اصلی | انتقال ژن برای مهار التهاب/بازسازی | حذف سلولهای سنسسانت | محیط سهبعدی برای سلول/دارو |
| مدت اثر | بلندمدت (سالها) | متوسط (ماهها) | متوسط تا بلند (۶-۱۲ ماه) |
| شواهد بالینی | اولیه (مایو، استنفورد) | پیشبالینی/اولیه (UBX0101) | پیشرفته (exosome hydrogels) |
| عوارض | پاسخ ایمنی | خفیف سیستمیک | تورم محلی |
| بهترین برای | OA شدید/پیری | OA مرتبط با سن | آسیبهای موضعی/کمتهاجمی |
سلولدرمانی و درمانهای تحملپذیر ایمنی (tolDC therapy، نانوپارتیکلها)
سلولدرمانی و درمانهای تحملپذیر ایمنی از جمله پیشرفتهای نوین در درمان آرتروز (به ویژه آرتریت روماتوئید) هستند که بر تنظیم سیستم ایمنی و بازسازی بافت تمرکز دارند. این رویکردها با استفاده از سلولهای خود بیمار یا مهندسیشده، التهاب را کاهش میدهند و تحمل ایمنی را القا میکنند تا حمله سیستم ایمنی به بافتهای سالم متوقف شود.
تا دسامبر ۲۰۲۵، مطالعات بالینی نشاندهنده ایمنی و اثربخشی اولیه این روشها هستند، اما بیشتر در مرحله آزمایشی قرار دارند. برای مثال، سلولدرمانی با سلولهای بنیادی یا CAR-T میتواند آسیب غضروف را ترمیم کند، در حالی که tolDC (سلولهای دندریتیک تحملپذیر) و نانوپارتیکلها التهاب را هدفمند مهار میکنند. این درمانها اغلب برای بیماران مقاوم به داروهای سنتی مناسب هستند و میتوانند کیفیت زندگی را بهبود بخشند.
سلولدرمانی (Cell Therapy)

سلولدرمانی شامل استفاده از سلولهای زنده برای ترمیم بافت یا تنظیم ایمنی است. در آرتروز، تمرکز بر سلولهای بنیادی مزانشیمی (MSCs) یا سلولهای مهندسیشده مانند CAR-T است که سیستم ایمنی را “ریست” میکنند.
- سلولهای بنیادی (Stem Cell Therapy): MSCs از مغز استخوان یا بافت چربی گرفته میشوند و به مفصل تزریق میشوند تا غضروف را بازسازی و التهاب را کاهش دهند. مطالعات ۲۰۲۵ نشان میدهند که بهینهسازی روشهای استخراج و تحویل، اثربخشی را افزایش داده است. موفقیت متوسط (تا ۷۰%) در کاهش درد گزارش شده، اما هنوز تحقیقاتی است.
- CAR-T Cell Therapy: این روش سلولهای T را مهندسی میکند تا سلولهای “سرکش” ایمنی را هدف قرار دهد. در ACR ۲۰۲۵، نتایج امیدوارکننده برای RA و SLE نشاندهنده رمیسیون بدون دارو است. ایمنی بهبود یافته و نسخههای “off-the-shelf” در حال توسعه هستند.
- سایر پیشرفتها: استفاده از AI و تکنیکهای تکسلولی برای شخصیسازی درمانها، مانند در لابراتوارهای CU Anschutz.
درمان tolDC (Tolerogenic Dendritic Cell Therapy)
tolDC سلولهای دندریتیک خود بیمار هستند که مهندسی میشوند تا تحمل ایمنی را القا کنند و حمله به مفاصل را متوقف نمایند. این روش ریشهای آرتریت روماتوئید را هدف قرار میدهد.
- مکانیسم: سلولها با آنتیژنهای خودی بارگذاری میشوند تا سیستم ایمنی را “آموزش” دهند. مطالعات نشان میدهند که tolDC التهاب را کاهش و تحمل را افزایش میدهد.
- پیشرفتهای ۲۰۲۵:پیشرفت بالینی AuToDeCRA-2 در نیوکاسل ایمنی و امکانپذیری را تأیید کرده و علائم زانو را در برخی بیماران تثبیت نموده است. تزریق داخلمفصلی با دوز ۱۰ میلیون سلول اثربخش بوده. همچنین، زیرگروههای tolDC اثرات متفاوتی روی T سلولها نشان دادهاند.
- کاربرد: برای RA متوسط تا شدید؛ در هلند و انگلستان در حال آزمایش است.
درمانهای مبتنی بر نانوپارتیکل (Nanoparticle-Based Therapies)
نانوپارتیکلها به عنوان حامل دارو یا القاگر تحمل ایمنی استفاده میشوند و داروها را هدفمند به محل التهاب میرسانند.
- مکانیسم: نانوپارتیکلها مانند لیپیدها یا پلیمرها، داروهای ضدالتهابی یا siRNA را حمل میکنند تا التهاب را کاهش و تحمل را القا کنند.
- پیشرفتهای ۲۰۲۵: نانوپارتیکلهای Agg-CLNP بیماری را پیشگیری و flareها را کنترل میکنند. Topas Therapeutics نانوپارتیکلهای ایمنی را به بالینی رسانده. همچنین، نانوپارتیکلهای بیومیمتیک با اکسوزومها التهاب را کاهش میدهند. PD-1 agonists و نانوپارتیکلهای tolerogenic تحمل را بازسازی میکنند.
- کاربرد: برای آرتریت روماتوئید و OA؛ کاهش عوارض سیستمیک و هدفمندی بالا.
مقایسه این درمانها در آرتروز (بر اساس شواهد ۲۰۲۵)
| ویژگی | سلولدرمانی (مانند CAR-T) | tolDC Therapy | نانوپارتیکلها |
|---|---|---|---|
| مکانیسم اصلی | ریست سیستم ایمنی و بازسازی | القا تحمل ایمنی | تحویل هدفمند دارو و تنظیم ایمنی |
| مدت اثر | بلندمدت (ریمیسیون بدون دارو) | متوسط (ماهها تا سال) | متوسط (نیاز به تکرار) |
| شواهد بالینی | ACR ۲۰۲۵، ایمنی بهبودیافته | AuToDeCRA-2، ایمنی و اثربخشی اولیه | Topas، Agg-CLNP، پیشگیری flare |
| عوارض | عفونت، پاسخ ایمنی | خفیف (تورم محلی) | کم (عوارض سیستمیک کاهشیافته) |
| بهترین برای | RA شدید مقاوم | RA متوسط | پیشگیری و کنترل التهاب |
این درمانها نویدبخش درمانهای ریشهای هستند، اما نیاز به مطالعات بیشتر دارند. اگر آرتریت روماتوئید دارید، با متخصص مشورت کنید.
کشفهای ژنتیکی و داروهای بازسازیشده (Repurposed drugs)
کشفهای ژنتیکی اخیر در زمینه آرتروز (به ویژه استئوآرتریت و آرتریت روماتوئید) نقش کلیدی در شناسایی اهداف درمانی جدید ایفا کردهاند. تا دسامبر ۲۰۲۵، مطالعات ژنومی گسترده (مانند GWAS) صدها نشانگر ژنتیکی جدید را شناسایی کرده که بسیاری از آنها به پروتئینهایی مرتبط هستند که توسط داروهای موجود (برای بیماریهای دیگر) هدف قرار میگیرند. این کشفها امکان بازسازی (repurposing) داروها را فراهم میکنند، یعنی استفاده از داروهای تأییدشده برای شرایط دیگر در درمان آرتروز، که میتواند زمان و هزینه توسعه داروهای جدید را کاهش دهد. این رویکردها بر پایه تنظیم سیستم ایمنی و جلوگیری از آسیب ساختاری تمرکز دارند و امید به درمانهای بیماری را افزایش میدهند.
کشفهای ژنتیکی اخیر
تحقیقات ژنتیکی در سالهای ۲۰۲۴-۲۰۲۵ پیشرفتهای چشمگیری داشته و عوامل ژنتیکی آرتروز را روشنتر کرده است:
- بزرگترین مطالعه GWAS: در یک متاآنالیز بر روی بیش از ۲ میلیون نفر (شامل ۵۰۰ هزار بیمار آرتروز)، ۹۶۲ نشانگر ژنتیکی شناسایی شد که ۵۱۳ مورد جدید بودند. این مطالعه ۷۰۰ ژن مرتبط با آرتروز را مشخص کرد و هشت فرآیند بیولوژیکی کلیدی (مانند ساعت circadian و عملکرد سلولهای گلیال) را برجسته نمود. این کشفها پتانسیل بازسازی صدها دارو را فراهم میکنند.
- سلولهای T جدید و ژنهای مرتبط با اختلالات ایمنی: با فناوری ReapTEC، انواع نادر سلولهای T helper و enhancerهای ژنتیکی مرتبط با RA، MS و آسم شناسایی شدند. این کشفها اهداف درمانی جدیدی برای تنظیم ایمنی ارائه میدهند.
- جهش ژنتیکی در پروتئین TRAF1: یک جهش خاص در TRAF1 پاسخ ایمنی بیشفعال را خاموش کرده و التهاب را در مدلهای موشی به طور چشمگیر کاهش میدهد. این کشف میتواند پایهای برای داروهای جدید در RA باشد.
- پیشرفتهای اپیژنتیک و ژنومی: بررسیهای سالانه استئوآرتریت نشاندهنده نقش اپیژنومیک در بافت چربی زیرکشککی و بیان ژنهای مرتبط با ویتامین K (مانند MGP) است. همچنین، روشهای آماری برای هممحلی ژنتیکی و miRNAها توسعه یافته.
این کشفها نه تنها علتشناسی آرتروز را روشن میکنند، بلکه به شناسایی اهداف دارویی جدید کمک میکنند.
داروهای بازسازیشده (Repurposed Drugs)
داروهای بازسازیشده داروهایی هستند که برای بیماریهای دیگر تأیید شدهاند اما بر اساس کشفهای ژنتیکی، برای آرتروز کاربرد پیدا میکنند. حدود ۱۰% ژنهای شناساییشده در GWAS توسط داروهای موجود هدف قرار میگیرند:
- داروهای ضدصرع برای استئوآرتریت : یک داروی صرع (مانند valproic acid یا مشابه) پتانسیل کند کردن تخریب مفصل در استئوآرتریت را نشان داده و میتواند بازسازی شود.
- مهارکنندههای T cell engagers از سرطان: این داروها (که برای سرطان مهندسی شدهاند) برای آرام کردن واکنشهای ایمنی در RA بازسازی میشوند، بدون سرکوب کامل سیستم ایمنی.
- داروهای سنولیتیک : برای سرطان، اما برای حذف سلولهای پیری در استئوآرتریت بررسی میشود و میتواند التهاب را کاهش دهد.
- سایر پتانسیلها: داروهای مرتبط با ویتامین K antagonists (مانند warfarin) در مطالعات مرتبط با پیشرفت استئوآرتریت بررسی شدهاند، اما نیاز به تحقیقات بیشتر دارند. همچنین، teplizumab (برای تأخیر دیابت نوع ۱) ممکن است برای بلوک اولیه RA بازسازی شود.
مقایسه کشفهای ژنتیکی و داروهای بازسازیشده (بر اساس شواهد ۲۰۲۵)
| ویژگی | کشفهای ژنتیکی | داروهای بازسازیشده |
|---|---|---|
| نمونه کلیدی | GWAS با ۹۶۲ نشانگر (۵۱۳ جدید) | داروهای ضدصرع، T cell engagers |
| هدف اصلی | شناسایی ژنها و فرآیندهای بیولوژیکی | استفاده از داروهای موجود برای اهداف جدید |
| مزایا | پایه برای درمانهای ریشهای | کاهش زمان توسعه، هزینه کمتر |
| چالشها | نیاز به ترجمه به بالینی | عوارض احتمالی، نیاز به آزمایشهای جدید |
| کاربرد | استئوآرتریت و RA (ژنهای ایمنی و پیری) | کنترل التهاب و تخریب مفصل |
این پیشرفتها امید به درمانهای مؤثرتر و شخصیسازیشده را افزایش میدهند، اما نیاز به مطالعات بالینی بیشتر دارند.
درمانهای در حال تحقیق و آینده (ژنسیلنسینگ، رادیوتراپی کمدوز)
درمانهای در حال تحقیق و آینده برای آرتروز (استئوآرتریت و آرتریت روماتوئید) بر پایه فناوریهای نوین مانند ژنتیک، نانوتکنولوژی و روشهای غیرتهاجمی تمرکز دارند. این رویکردها اغلب در مرحله کارآزماییهای بالینی (Phase I-III) هستند و هدف آنها نه تنها کنترل علائم، بلکه اصلاح ریشهای بیماری (disease-modifying) است. تا دسامبر ۲۰۲۵، پیشرفتهای چشمگیری گزارش شده، اما بسیاری نیاز به تأییدهای بیشتر دارند. در این بخش، به ژنسیلنسینگ (مانند siRNA و CRISPR) و رادیوتراپی کمدوز میپردازیم، همراه با نگاهی به سایر درمانهای آینده. این درمانها میتوانند جایگزین جراحی یا داروهای سنتی شوند، اما همیشه تحت نظارت متخصص ارزیابی شوند.
ژنسیلنسینگ (Gene Silencing)
ژنسیلنسینگ با خاموش کردن ژنهای التهابی یا تخریبی (مانند IL-1 یا TNF-α) التهاب و آسیب غضروف را کاهش میدهد. این روش از فناوریهایی مانند siRNA (small interfering RNA)، CRISPR-Cas9 و نانوتکنولوژی استفاده میکند و پتانسیل درمان ریشهای را دارد.
- مکانیسم: siRNA یا CRISPR ژنهای مشکلساز را خاموش میکنند؛ نانوکریرها (nanocarriers) دارو را مستقیم به مفصل میرسانند تا عوارض سیستمیک کاهش یابد.
- پیشرفتهای ۲۰۲۵: سیستم جدید peptide-siRNA برای درد و التهاب استئوآرتریت ، که در دانشگاه بیرمنگام توسعه یافته و درد را در منبع هدف قرار میدهد. شرکت Genascence با ژندرمانی بلوککننده IL-1 نتایج مثبت اولیه در استئوآرتریت نشان داده. همچنین، CRISPR برای مدولاسیون مسیرهای ژنتیکی در مدلهای حیوانی موفق بوده و ممکن است برای RA گسترش یابد.
- کاربرد: مناسب برای استئوآرتریت و RA مقاوم؛ در Phase I-II، با نتایج امیدوارکننده در کاهش درد و حفظ غضروف.
- عوارض: پاسخ ایمنی یا عفونت نادر؛ نیاز به تحقیقات بیشتر برای ایمنی بلندمدت.
رادیوتراپی کمدوز (Low-Dose Radiotherapy – LDRT)

رادیوتراپی کمدوز با دوزهای پایین (کمتر از ۶ Gy) التهاب را کاهش میدهد و درد را تسکین میبخشد، بدون آسیب به بافتهای سالم. این روش قدیمی اما بازسازیشده، گزینهای غیرتهاجمی برای بیماران مسن یا مقاوم به دارو است.
- مکانیسم: تابش کمدوز ماکروفاژها را مدوله کرده و سایتوکینهای التهابی را کاهش میدهد؛ اغلب در ۶-۱۰ جلسه (۰.۵-۱ Gy هر بار) انجام میشود.
- پیشرفتهای ۲۰۲۵: کارآزمایی placebo-controlled ASTRO نشان داد LDRT درد زانو استئوآرتریت را به طور قابل توجه کاهش میدهد. مراکز مانند Upstate و Advocate Radiation Oncology برنامههای LDRT را برای درد مزمن مفاصل گسترش دادهاند، با تسکین بلندمدت (تا ۱۲ ماه) و عوارض کم. مطالعه NIH اثرات ضدالتهابی LDRT را تأیید کرده.
- کاربرد: برای استئوآرتریت زانو، دست یا لگن؛ گزینه محافظهکارانه به جای جراحی.
- عوارض: خفیف (قرمزی پوست موقت)؛ ریسک سرطان بسیار پایین با دوزهای کم.
سایر جدیدترین درمالن های آرتروز
علاوه بر موارد فوق، تحقیقات ۲۰۲۵ بر درمانهای شخصیسازیشده تمرکز دارد:
- رشد فاکتورهای جدید: درمانهای growth factor برای افزایش ضخامت غضروف در OA.
- داروهای جدید مانند rosnilimab: برای RA، با حذف سلولهای ایمنی بیشفعال در ACR ۲۰۲۵.
- بیولوژیکهای نوین مانند sonelokimab: برای آرتریت پسوریاتیک، با اثربخشی بالا.
- PRP پیشرفته: برای استئوآرتریت زانو، با شواهد جدید ۲۰۲۵.
- دقت پزشکی: استفاده از GWAS برای شناسایی ۷۰۰ ژن مرتبط و بازسازی داروها.
مقایسه درمانهای در حال تحقیق و آینده (بر اساس شواهد ۲۰۲۵)
| ویژگی | ژنسیلنسینگ (siRNA/CRISPR) | رادیوتراپی کمدوز (LDRT) | سایر آینده (مانند rosnilimab/PRP) |
|---|---|---|---|
| مکانیسم اصلی | خاموش کردن ژنهای التهابی | کاهش التهاب با تابش کمدوز | تنظیم ایمنی/بازسازی بافت |
| مدت اثر | بلندمدت (سالها) | متوسط تا بلند (۶-۱۲ ماه) | متوسط (نیاز به تکرار) |
| شواهد بالینی | Phase I-II (Genascence، بیرمنگام) | کارآزماییهای موفق (ASTRO، NIH) | ACR ۲۰۲۵، GWAS-based |
| عوارض | پاسخ ایمنی نادر | خفیف موضعی | عفونت یا تورم کم |
| بهترین برای | OA/RA مقاوم ریشهای | درد مزمن OA بدون جراحی | RA/PsA شخصیسازیشده |
این درمانها آینده امیدوارکنندهای برای آرتروز ترسیم میکنند، اما نیاز به تأیید FDA/EMA دارند.
سبک زندگی و پیشگیری (ورزش، تغذیه، مدیریت وزن)
تغییرات سبک زندگی نقش کلیدی در پیشگیری از پیشرفت آرتروز و کاهش علائم آن دارند. حتی در افراد مبتلا به استئوآرتریت یا آرتریت روماتوئید، این اقدامات میتوانند درد را کاهش دهند، عملکرد مفاصل را حفظ کنند و نیاز به دارو یا جراحی را به تأخیر بیندازند. ورزش، تغذیه مناسب و مدیریت وزن قویاً توصیه میشوند و اغلب به عنوان پایه درمان در نظر گرفته میشوند.
ورزش و فعالیت بدنی
ورزش مناسب نه تنها عضلات اطراف مفاصل را تقویت میکند، بلکه التهاب را کاهش میدهد، دامنه حرکتی را حفظ میکند و وزن را کنترل میکند.
- انواع توصیهشده:
- ورزشهای هوازی کمفشار: پیادهروی، شنا، دوچرخهسواری یا الیپتیکال (۳۰ دقیقه، ۵ روز در هفته).
- تمرینات تقویتی: وزنههای سبک یا باند مقاومتی برای تقویت عضلات چهارسر ران، همسترینگ و هسته بدن.
- تمرینات تعادلی و انعطافپذیری: یوگا، تایچی یا پیلاتس (کاهش خطر افتادن و بهبود تعادل).
- مزایا: کاهش ۲۰-۳۰% درد در استئوآرتریت زانو، بهبود سفتی صبحگاهی در RA، افزایش کیفیت زندگی.
- نکته مهم: از ورزشهای پرضربه (دویدن شدید، پریدن) در استئوآرتریت مفاصل تحملکننده وزن پرهیز کنید. همیشه با فیزیوتراپیست برنامه شخصیسازیشده تنظیم کنید.
تغذیه و رژیم غذایی ضدالتهابی

تغذیه مناسب التهاب سیستمیک را کاهش میدهد و به حفظ وزن سالم کمک میکند.
- مواد غذایی توصیهشده:
- رژیم مدیترانهای: غنی از ماهی (امگا-۳)، روغن زیتون، میوهها، سبزیجات، آجیل و غلات کامل.
- منابع امگا-۳: ماهیهای چرب (سالمون، ساردین)، گردو، بذر کتان (کاهش التهاب در آرتریت روماتوئید).
- آنتیاکسیدانها: توتها، سبزیجات برگسبز، زردچوبه (کورکومین)، زنجبیل.
- ویتامین D و کلسیم: برای سلامت استخوان (لبنیات کمچرب، سبزیجات برگسبز، مکمل در صورت کمبود).
- مواد غذایی محدودشده:
- شکر، غذاهای فرآوریشده، چربیهای ترانس و گوشت قرمز (افزایش التهاب).
- در آرتریت روماتوئید: برخی بیماران به گلوتن یا لبنیات حساسیت دارند (با آزمایش شناسایی شود).
- شواهد ۲۰۲۵: رژیم مدیترانهای درد و فعالیت بیماری را در آرتریت روماتوئید کاهش میدهد و پیشرفت OA را کند میکند.
مدیریت وزن
چاقی یکی از مهمترین عوامل خطر قابل اصلاح در آرتروز است، به ویژه استئوآرتریت زانو و لگن.
- تأثیر وزن:
- هر کیلوگرم اضافه وزن، ۴ کیلوگرم فشار بیشتر روی زانو وارد میکند.
- کاهش ۵-۱۰% وزن بدن میتواند درد زانو را تا ۵۰% کاهش دهد و پیشرفت بیماری را کند کند.
- روشهای مؤثر:
- ترکیب رژیم غذایی سالم + ورزش منظم.
- هدف واقعبینانه: کاهش ۰.۵-۱ کیلوگرم در هفته.
- مزایا در آرتریت روماتوئید: کاهش وزن التهاب سیستمیک (CRP و ESR) را کاهش میدهد و پاسخ به داروها را بهبود میبخشد.
مقایسه تأثیر تغییرات سبک زندگی در دو نوع آرتروز
| اقدام | استئوآرتریت (OA) | آرتریت روماتوئید (RA) |
|---|---|---|
| ورزش | بسیار مؤثر (تقویت عضلات، کاهش فشار) | مؤثر (کاهش سفتی، حفظ عملکرد) |
| کاهش وزن | قویترین تأثیر (کاهش فشار مکانیکی) | مفید (کاهش التهاب سیستمیک) |
| تغذیه ضدالتهابی | متوسط (مدیترانهای، امگا-۳) | قوی (کاهش فعالیت بیماری) |
| پیشگیری | جلوگیری از پیشرفت در افراد در معرض خطر | کاهش flare-up و بهبود پاسخ درمانی |
| شواهد توصیه | قوی (ACR/OARSI) | قوی (EULAR) |
نکات عملی برای شروع
- با پزشک یا فیزیوتراپیست مشورت کنید تا برنامه شخصیسازیشده دریافت کنید.
- تغییرات را تدریجی اعمال کنید (مثلاً ۱۰ دقیقه پیادهروی روزانه شروع شود).
- از اپلیکیشنها یا گروههای حمایتی برای پیگیری استفاده کنید.
- سیگار را ترک کنید (سیگار پیشرفت آرتریت روماتوئید را تسریع و پاسخ درمانی را کاهش میدهد).
این تغییرات ساده اما قدرتمند میتوانند تأثیر بیشتری از بسیاری داروها داشته باشند و پایهای برای تمام درمانهای دیگر هستند.
نتیجهگیری: امید به آیندهای بدون درد آرتروز
آرتروز، چه از نوع استئوآرتریت (ساییدگی مفاصل) و چه آرتریت روماتوئید (التهابی خودایمنی)، همچنان یکی از شایعترین علل درد مزمن و ناتوانی در جهان است. اما خبر خوب این است که در سال ۲۰۲۵، دیگر فقط به کنترل علائم محدود نیستیم؛ پیشرفتهای چشمگیر علمی ما را به سمت درمانهای اصلاحکننده بیماری (disease-modifying) و حتی بازسازیکننده بافت سوق داده است.
امروزه میدانیم که:
- درمانهای سنتی مانند داروهای ضدالتهاب، فیزیوتراپی و کاهش وزن همچنان پایه مدیریت موفق هستند.
- تزریقهای مفصلی (به ویژه PRP و هیالورونیک اسید) میتوانند ماهها تسکین قابل توجه ایجاد کنند.
- داروهای هدفمند جدید مانند مهارکنندههای JAK و بیولوژیکهای IL-23 برای بیماران التهابی، رمیسیون طولانیمدت فراهم میکنند.
- روشهای نوین مانند تحریک عصبی واگوس، سلولدرمانی، ژندرمانی، سنولیتیکها و هیدروژلهای تزریقی، در حال تغییر پارادایم درمان از “کنترل” به “ترمیم” هستند.
- کشفهای ژنتیکی عظیم و بازسازی داروهای موجود، سرعت توسعه درمانهای شخصیسازیشده را چندین برابر کردهاند.
- و در نهایت، تغییرات ساده سبک زندگی (ورزش منظم، رژیم ضدالتهابی و مدیریت وزن) قدرتمندترین ابزار پیشگیری و کند کردن پیشرفت بیماری باقی میمانند.
آینده روشن است: در دهه پیش رو، احتمالاً شاهد درمانهایی خواهیم بود که نه تنها درد را از بین میبرند، بلکه غضروف آسیبدیده را بازسازی میکنند، سیستم ایمنی را دوباره تنظیم میکنند و حتی از بروز بیماری در افراد در معرض خطر جلوگیری میکنند.
پیام نهایی: اگر شما یا عزیزانتان با آرتروز زندگی میکنید، ناامید نشوید. تشخیص زودهنگام، مدیریت فعال و پیگیری پیشرفتهای علمی میتواند تفاوت بزرگی ایجاد کند. حتماً با یک متخصص روماتولوژی مشورت کنید تا برنامه درمانی شخصیسازیشدهای دریافت کنید که ترکیبی از درمانهای اثباتشده امروز و گزینههای نوین فردا باشد.
زندگی بدون درد مفاصل دیگر یک آرزو نیست – یک هدف دستیافتنی است.


Leave Your Comment